酸性氧化物和碱性氧化物相互作用可生成含氧酸盐,而硫代硫酸盐可由酸性的非金属硫化物与碱性的金属硫化物作用制得。
如:3Na2S+As2S3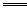 2Na3AsS3(硫代亚砷酸钠),试写出下列反应的化学方程式:
2Na3AsS3(硫代亚砷酸钠),试写出下列反应的化学方程式:
(1)Na2S与As2S5反应: 。
(2)CaS与As2S3反应: 。
(3)As2S3和As2O3相似,具有还原性,Na2S2和Na2O2相似,具有氧化性,则As2S3与Na2S2作用的化学方程式为 。
硫化氢(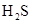 )分子中,两个H—S键的夹角接近90°,说明
)分子中,两个H—S键的夹角接近90°,说明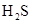 分子的空间构型为;二氧化碳(
分子的空间构型为;二氧化碳( )分子中,两个C=O键的夹角是180°,说明
)分子中,两个C=O键的夹角是180°,说明 分子的空间构型为;甲烷(
分子的空间构型为;甲烷(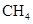 )分子中,两个相邻C—H键的夹角是109°28′,说明CH4分子的空间构型为。
)分子中,两个相邻C—H键的夹角是109°28′,说明CH4分子的空间构型为。
空格处是横线
2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想。
运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物。已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键。
(1)该氮氢化合物的电子式为。
(2)若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,写出该反应的化学方程式。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出上述氮氢化合物通入足量盐酸时,发生反应的化学方程式。
在一定条件下,某元素的氢化物X可完全分解为两种单质:Y和Z。若已知:
①反应前的X与反应后生成的Z的物质的量之比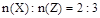
②单质Y的分子为正四面体构型。
请填写下列空白。
(1)单质Y是___________,单质Z是___________(填写名称或分子式)。
(2)Y分子中共含___________个共价键。
(3)X分解为Y和Z的化学方程式为:______________________。
在HCl分子中,由H原子的一个轨道与Cl原子的一个轨道形成一个键;在Cl2分子中两个Cl原子以轨道形成一个键。
乙烯分子中C-C之间有个σ键,个π键。乙烯易发生加成反应是因为分子中C-C之间的一个键易断裂。