有A、B、C、D、E五种主族元素,原子序数依次增大,且不超过36。已知B、C、D同周期,A与D同主族,C与E同主族。A原子最外层电子数为内层电子数的3倍,C原子的内层电子总数为最外层电子数的2倍,B在同周期主族元素中原子半径最大。
(1)写出B2A2的电子式:______________________________________________________。
(2)已知E2A3为有剧毒的白色固体,微溶于水,易溶于浓HCl和NaOH溶液。写出E2A3分别和浓HCl和NaOH溶液反应的化学方程式:
E2A3与浓HCl反应:______________________________________________________________
E2A3与NaOH溶液反应:___________________________________________________________
(3)取E2A3的HCl溶液,通入D的氢化物,发生复分解反应,析出一种黄色沉淀,其反应的化学方程式为:______________________________________________________________。
现有反应:CO(g)+ H2O(g) CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。
CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。
(1)若升高温度到950℃时,达到平衡时K__ ___1(填“>”、“<”或“=”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、1.0mol CO2和 x molH2,则:
①当x=5.0时,上述平衡向_______(填“正反应”或“逆反应”)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是________。
(3)在850℃时,若设x=5.0 mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a _______ b(填“>”、“<”或“=”)。
现有A、B两种链状饱和一元醇的混合物0.3 mol,其质量为13.8g。已知①A和B碳原子数均不大于4,且A<B;②A和B分子中均不含有支链,且都能被催化氧化生成醛。
(1)混合物中A可能的分子式;B可能的分子式。
(2)若n(A):n(B)=1:1时,A的名称B的名称。
(3)若n(A):n(B)≠1:1时,A的结构简式为;
B的结构简式为。则n(A)∶n(B) =。
按以下步骤可从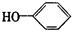 合成
合成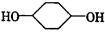 (部分试剂和反应条件已去).
(部分试剂和反应条件已去).
请回答下列问题:
(1)B、F的结构简式为:BF。
(2)反应①~⑦中属于消去反应的是(填代号)。
(3)根据反应 ,写出在同样条件下
,写出在同样条件下
CH2=CH—CH=CH2与等物质的量 发生加成反应的化学方程式:
发生加成反应的化学方程式:
。
(4)写出第④步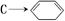 的化学方程式(有机物写结构简式,注明反应条件).
的化学方程式(有机物写结构简式,注明反应条件).
。
(5)A—G这七种有机物分子中含有手性碳原子的是(填序号) 。
(6)核磁共振谱是测定有机物分子结构最有用的工具之一。在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的结构式为: ,其PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是。
,其PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是。
A.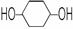 B.
B.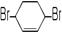 C.
C. D.
D.
(8分)按要求完成下列问题
(1)甲基的电子式________ _____
(2)通式为CnH2n+2的最简单同系物的分子式
(3)相对分子质量为72且沸点最低的烷烃的结构简式___________________
(4)1、3-丁二烯的键线式
(4分)下列叙述正确的是________________(选对一个给2分,多选、错选一个扣1分,本题不出现负分)。
| A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗。 |
| B.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体。 |
| C.浓溴水滴入苯酚溶液中立即产生2,4,6-三溴苯酚的白色沉淀。 |
| D.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,但该现象不能说明苯和溴的取代反应就是放热反应。 |
E.分离沸点相差30℃以上的混溶液体,应采用的方法是分馏
F.实验室使用体积比为1:3的浓硫酸与乙醇的混合溶液制乙烯时,为防加热时反应混合液出现暴沸现象,除了要加沸石外,还应注意缓慢加热让温度慢慢升至170℃。
G.除去混在苯中的少量苯酚,加入过量溴水,过滤。