CCTV对“南澳一号”沉船的考古进行了两个小时的现场直播,从沉船中发现了大量宋代精美瓷器,体现了灿烂的中华文明。青花瓷胎体的原料——高岭土[Al2Si2O5(OH)x],可掺进瓷石制胎,青花瓷釉料的成分主要是钾长石(KAlSi3O8),在1 300℃左右一次烧成的釉可形成精美的青花瓷。
(1)下列说法正确的是 。
A.高岭土分子中x=2
B.钾长石能完全溶解在盐酸中形成澄清的溶液
C.烧制青花瓷过程中发生了复杂的物理变化和化学变化
D.青花瓷、玻璃、水泥都属于硅酸盐产品
(2)在“南澳一号”考古直播过程中,需用高纯度SiO2制造的光纤。如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。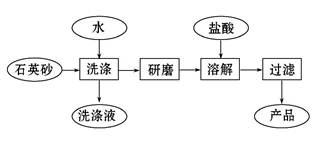
①洗涤石英砂的目的是
。
②二氧化硅与氢氧化钠溶液反应的离子方程式是
。
③工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是 。
A.制造粗硅时的反应为2SiO2+5C Si+SiC+4CO↑
Si+SiC+4CO↑
B.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
C.纯净的SiO2只能用于制造光导纤维
(3)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,其生产过程示意图如下: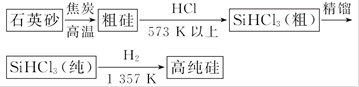
①写出由纯SiHCl3制备高纯硅的化学反应方程式
。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式
;
H2还原SiHCl3过程中若混入O2,可能引起的后果是
。
水杨酸是合成阿斯匹林的重要原料。水杨酸的结构简式为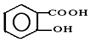
请回答下列问题:
(1)请写出水杨酸中除苯环外具有的官能团的名称;
(2)请写出与水杨酸互为同分异构体,既属于酚类又属于酯类化合物的结构简式:;
(3)写出水杨酸与碳酸氢钠反应的化学方程式:
(4)在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林如下图所示,1摩尔阿司匹林与氢氧化钠完全反应需要氢氧化钠摩尔。
(5)阿斯匹林药片需要保存在干燥处,受潮的药片易变质不宜服用;检验受潮药片是否变质的试剂是(只选一种试剂即可)
现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;0. 96 g D的单质跟足量盐酸反应,生成D3+和1.2 L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构。
(1) 写出元素符号:
A,C,E。
(2) B、D的最高价氧化物对应水化物相互反应的离子方程式为:
。
(3) 用电子式表示C与E形成E2C的过程:。
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| A |
有三个电子层,且K、M层电子数之和等于L层电子数 |
| B |
最外层电子数是次外层电的2倍 |
| C |
常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| D |
元素最高正价是+7价 |
(1)写出A元素在周期表中的位置,B元素的名称。
(2)写出C元素的单质的电子式。
(3)元素D与元素A相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是(填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
(4)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是(写化学式)。
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 二 |
① |
② |
||||||
| 三 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 四 |
⑨ |
⑩ |
⑴在这些元素中,化学性质最不活泼元素的原子结构示意图为。
⑵得电子能力最强的是地壳中含量最多的金属元素是。
⑶用电子式表示②与④形成化合物的过程 。
⑷这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是,呈两性的氢氧化物是。
⑸比较②③④⑦形成的简单离子半径的大小 。
⑹某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L。则HXR的相对分子量为 ;HXR的化学式为 。
碱金属元素在科学研究和生产生活中有着广泛用途。
(1)锂是最轻的金属,如果用锂做一架飞机,两个人就可以抬动。锂在元素周期表中的表示如右图所示,填写以下空格。
①Li在元素周期表中的位置:。
②6.941的意义: __________________________。
(2)光电管是利用碱金属铯受到光照射时能形成电流这一光电效应的性质制成的。
①完成铯的原子结构示意图:
②下列有关铯的说法正确的是________。
| A.其单质在常温下与水反应不如钠剧烈 |
| B.其原子半径比钾原子半径小 |
| C.其氢氧化物的水溶液不能使氢氧化铝溶解 |
| D.其碳酸盐易溶于水 |