1 mol Cu和1 mol碳分别与足量的浓硫酸反应,下列叙述正确的是( )
| A.消耗的硫酸量相同 | B.消耗的硫酸量不同 |
| C.被还原的硫酸量相同 | D.被还原的硫酸量不同 |
上海世博园地区的一座大型钢铁厂搬迁后,附近居民将不再受到该厂产生的红棕色烟雾的困扰。你估计这一空气污染物可能含有( )
| A.FeO粉尘 | B.Fe2O3粉尘 | C.Fe粉尘 | D.碳粉 |
光导纤维被认为是20世纪最伟大的发明之一,它使信息高速公路在全球迅猛发展,它的发明者是被誉为“光纤之父”的华人科学家高锟。光导纤维的主要成分是( )
| A.SiO2 | B.CaCO3 | C.Na2SiO3 | D.CaSiO3 |
高铁酸钾(K2FeO4)和二氧化氯(ClO2)都是高效水处理剂,其工业制备的反应原理分别为 2Fe(OH)3+3 KClO+4KOH=2K2FeO4+3KCl+5H2O
2KClO3+ Na2SO3 +H2SO4=2ClO2 + Na2SO4+ K2SO4+ H2O
下列说法中,正确的是()
| A.上述两个反应中, KClO3做氧化剂,KClO 做还原剂 |
| B.ClO2做水处理剂原理和明矾相同 |
| C.K2FeO4用于杀菌后其还原产物还可用作净水剂 |
| D.制备等物质的量的K2FeO4和ClO2,转移的电子数之比为1 : 1 |
在一定温度下,Na2CO3溶液中存在水解平衡:CO32-+H2O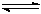 HCO3-+OH-。下列说法中,正确的是()
HCO3-+OH-。下列说法中,正确的是()
A.升高温度,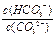 减小 减小 |
B.通入CO2,平衡向正反应方向移动 |
| C.稀释溶液,Na2CO3水解程度增大,水解平衡常数增大 |
| D.加入NaOH固体,平衡向逆反应方向移动,溶液pH减小 |
若NA代表阿伏加德罗常数,则下列叙述正确的是() 
A.16g氧气和臭氧的混合物中原子的数目0.5NA |
B.1mol Cl2与足量的铁完全反应,转移的电子数为2NA |
C.1 L 0.5mol·L-1AlCl3溶液中含有的Al3+数目为0.5NA |
D.在标准状况下,22.4L HCl与22.4L H2O2所含有的电子数均为18 NA |