(14分)今有三种物质AC2、B2C2、AD4,元素A的最高正价和负化合价绝对值相等,元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;
元素D的负一阶阴离子电子层结构与氩原子相同,则:
(1)A、B、C、D的元素符号为A_______________、B_______________、C_______________、D_______________。
(2)AC2、B2C2、AD4的电子式分别为_______________、______________、______________。
(3)AC2的分子空间构型是_______________,属于_______________ (填“极性”或“非极性”)分子。AD4分子的空间构型是______________,属于_____________(填“极性”或“非极性”)分子。
(4)B2C2中既含有_______________键,又含有_______________键,属于_______________ (填“离子”或“共价”)化合物。
芳香族化合物A有如下图的转化关系: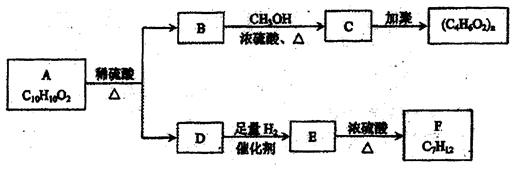
已知D能与NaOH溶液反应,E转化为F时,产物只有一种结构,且能使溴的四氯化碳溶液褪色。请 回答下列问题:
回答下列问题:
(1)D中官能团的名称为
(2)B的分子式是
(3)A、F的结构简式:AF
(4)写出B→C、E→F的化学反应方程式,并注明反应类型
B→C:()
E→F:( )
)
(5)符合下列3个条件的A的同分异构体有多种
①苯环含有的二取代结构处于对位
②遇FeCl2溶液不变色
③能发生银镜的
请写出其中两种的结构简式
短周期元素A、B、C、D、E在元素周期表中的 位置如下图所示,其中B元素形成的化合物在自然界中的种类最多。
位置如下图所示,其中B元素形成的化合物在自然界中的种类最多。
请回答下列问题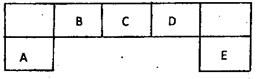

(1)描述D在元素周期表中的位置:
(2)比较A、C、D元素简单离子半径的大小:____>>(填微粒符号)
(3)F与D同主族且相邻,请说出D的氢化物比F的氢化物稳定的根本原因:
(4)C的氢化物与其最高价氧化物对应的水化物反应,产物溶于水呈性,用离子方程式解释原因。
(5)D原子与氢原子可形成10电子阳离子,写出该阳离子的电子式
(6)E的最高价氧化物的水化物的化学式为。E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,该反应的化学反应方程式为
某烷烃A蒸气的密度是相同状况下氢气密度的64倍,经测定得知分子中共含有6个甲基。
(1)若A不可能是氢气与烯烃加成的产物,A的结构简式是:。
(2)若A是烯烃与氢气加成的产物,A的结构简式是:。
已知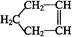 可简写为
可简写为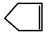 。降冰片烯的分子结构可表示为:
。降冰片烯的分子结构可表示为: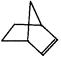
(1)降冰片烯属于__________。
A环烃 B不饱和烃 C烷烃 D芳香烃
(2)降冰片烯的分子式为__________。
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为__________。
(4)降冰片烯不具有的性质__________。
A能溶于水 B能发生氧化反应
C能发生加成反应 D常温常压下为气体
写出下列反应的化学反应方程式,并判断其反应类型。
①乙醇的催化氧化:,属于反应;
②由苯制取溴苯:,属于反应;
③由苯制取环己烷:,属于反应;
④由乙烯制取聚乙烯:,属于反应;