某固体可能由KNO3、Cu(NO3)2、AgNO3中的一种或几种组成。已知其热分解反应方程式为:
2KNO3 2KNO2+O2↑
2KNO2+O2↑
2Cu(NO3)2 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
现将该固体物质加热分解,得到n L气体,将这些气体通过足量的水后还剩余 L气体(气体体积在相同状态下测定,且不考虑NO2聚合成N2O4的情况)。
L气体(气体体积在相同状态下测定,且不考虑NO2聚合成N2O4的情况)。
(1)若该固体中只含一种物质,则该物质是__________(填化学式,下同);
(2)若该固体中含两种物质,则该两种物质是______、______,其物质的量之比为______;
(3)若该固体中含全部三种物质,则三种物质的物质的量之比为________。
(12分)
(1)实验室在临时配制一些FeCl2的溶液时,常将氯化亚铁固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,是为了。稀释后还需要加入一些铁粉,其目的是,相关反应的离子方程式为。
(2)氯化铁水溶液呈性 ,原因是(用离子方程式表示):
_________________________ 。把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是。如果要从氯化铁溶液得到纯氯化铁固体,常采用的方法是。
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答: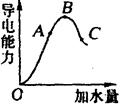
(1)“O”点导电能力为“0”的理由是
。
(2)A、B、C三点pH由大到小的顺序是__________________。
(3)A、B、C三点电离度最大的是_____________。
请用下图的装置设计一个实验,以测定SO2转化为SO3的转化率。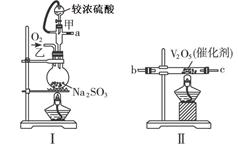
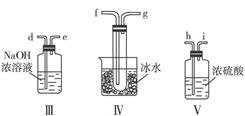
(1)这些装置的连接顺序(按气体从左到右的方向)是___________。(填各接口的编号)
(2)实验时甲仪器的作用与原理是____________________________________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是________________________________。
(4)Ⅳ处观察到的现象是___________________________。
(5)在Ⅰ处用大火加热烧瓶时SO2的转化率会__________。(填“填大”“不变”或“减小”)
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为______________。
A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中A、D及C、F分别是同一主族元素。A、C两元素可形成原子个数之比为2︰:1、1︰1型化合物。B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数。F元素的最外层电子数是次外层电子数的0.75倍。请回答:
(1)D与F形成D2F的电子式为______________;A、C、D三种元素组成的化合物含有化学键的类型是________________;
(2)由E、F两种元素组成的化合物1 mol跟由A、C、D三种元素组成的化合物的溶液发生反应,消耗后者物质的量最大值为___________ mol。
(3)A、C、F间形成的甲、乙两种微粒,甲有18个电子,乙有10个电子,它们均为负一价双原子阴离子,则甲与乙反应的离子方程式为_________________________________ 。
(4)工业上在高温的条件下,可 以用A2C和BC反应制取单质A2。在等体积的Ⅰ、Ⅱ两个密闭容器中分别充入1 mol A2C和1 mol BC、2 mol A2C和2 mol BC。一定条件下,充分反应后分别达到平衡(两容器温度相同)。下列说法正确的是________________ 。
以用A2C和BC反应制取单质A2。在等体积的Ⅰ、Ⅱ两个密闭容器中分别充入1 mol A2C和1 mol BC、2 mol A2C和2 mol BC。一定条件下,充分反应后分别达到平衡(两容器温度相同)。下列说法正确的是________________ 。
A.达到平衡所需要的时间:Ⅰ>Ⅱ B.达到平衡后A2C的转化率:Ⅰ=Ⅱ
C.达到平衡后BC的物质的量:Ⅰ>Ⅱ D.达到平衡后A2的体积分数:Ⅰ<Ⅱ
E.达到平衡后吸收或放出的热量:Ⅰ=Ⅱ F.达到平衡后体系的平均相对分子质量:Ⅰ<Ⅱ
超细铜粉主要应用于导电材料、催化剂等领域中。超细铜粉的某制备方法如下:
试回答下列问题:
(1)下列关于[Cu(NH3)4]SO4的说法中,正确的有__________。(填字母序号)
| A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键 |
| B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子 |
| C.[Cu(NH3)4]SO4的组成元素中第一电离能最大的是氧元素 |
| D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体 |
(2)NH4CuSO3中的金属阳离子的核外电子排布式为_______________。
(3)SO2–3 离子中S硫原子的杂化方式为________,与其互为等电子体的一种分子的分子式是___________。
(4)NH3易液化的原因是___________________。
(5)右图是铜的某种氧化物的晶胞结构示意图,由此可确定该氧化物的化学式_____。
(6)NH4CuSO3与硫酸微热反应的离子方程式为__________________________。