已知反应NH4NO3 HNO3+N2+H2O(未配平),被氧化的N原子与被还原的N原子的物质的量之比是( )
HNO3+N2+H2O(未配平),被氧化的N原子与被还原的N原子的物质的量之比是( )
| A.3∶5 | B.5∶3 | C.2∶5 | D.1∶2 |
关于SO2的叙述中,正确的是
| A.SO2的摩尔质量是64 g |
| B.1mol SO2中所含分子数约为6.02×1023 |
| C.1 mol SO2的质量是64g / mol |
| D.常温常压下,1 mol SO2的体积为22.4 L |
下列反应中,属于氧化还原反应的是
A.2 H2O2 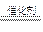 2 H2O + O2↑ 2 H2O + O2↑ |
B.2 Al(OH)3  Al2O3 + 3 H2O Al2O3 + 3 H2O |
| C.FeO + 2 HCl = FeCl2+ H2O | D.CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl |
摩尔是
| A.物质的数量单位 | B.物质的质量单位 |
| C.既是物质的数量单位又是物质的质量单位 | D.物质的量的单位 |
氧化还原反应的实质是
| A.氧元素的得失 | B.化合价的升降 |
| C.电子的得失或偏移 | D.分子中原子的重新组合 |
下列物质属于非电解质的是
| A.CO2 | B.NaOH | C.NaCl | D.H2SO4 |