从下列实验事实所得出的相应结论正确的是
| |
实验事实 |
结论 |
| ① |
将某气体通入品红溶液中,品红溶液褪色 |
该气体一定是SO2 |
| ② |
将燃烧的镁条放入CO2中能继续燃烧 |
还原性:Mg>C |
| ③ |
NaHCO3溶液与Na[Al(OH)4]溶液混合产生白色沉淀 |
酸性:HCO3->Al(OH)3 |
| ④ |
常温下白磷可自然而氮气需在放电时才于氧气反应 |
非金属性:P>N |
| ⑤ |
某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该晶体中一定有NH4+ |
A.②③⑤ B.①②③ C.③④⑤ D.①③⑤
下列化学反应,不属于氧化还原反应的是()
A.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 |
B.Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
C.3Fe+2O2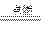 Fe3O4 Fe3O4 |
D.CaCO3 CaO + CO2↑ CaO + CO2↑ |
NA表示阿伏加德罗常数,下列叙述正确的是()
| A.22.4L的N2和CO所含分子数均为NA |
| B.1.7g H2O2中含有的电子数为0.9 NA |
| C.1mol Na2SO4固体中含离子总数为4 NA |
| D.标准状况下,2.24L CCl4所含分子数为0.1 NA |
下列化学变化中,需加入氧化剂才能实现的是()
| A.C→CO2 | B.CO2→CO | C.CuO→Cu | D.H2SO4→BaSO4 |
下列实验操作中,不正确的是() 

熄灭酒精灯取用固体粉末读液体体积滴加液体
ABCD
对下列物质进行的分类正确的是()
| A.纯碱、烧碱均属于碱 | B.CuSO4·5H2O属于纯净物 |
| C.凡能电离出H+的化合物均属于酸 | D.盐类物质一定含有金属阳离子 |