铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生4480 mL的NO2气体和336 mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的NaOH溶液,生成沉淀的质量为( )
| A.9.02 g | B.8.51 g | C.8.26 g | D.7.04 g |
下列离子方程式与所述事实相符且正确的是
A.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液: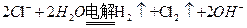 |
B.用稀硝酸清洗做过银镜反应的试管: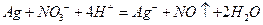 |
C.向FeBr2溶液中通入过量的 : :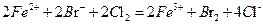 |
| D.在强碱性溶液中,次氯酸钠将Mn2+氧化成Mn02: |
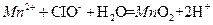
下列化学实验事实及解释都正确的是
| A.向Na2S03溶液中加入硝酸酸化的BaCl2溶液,有白色沉淀出现,说明Na2S03溶 液已经变质 |
| B.向皂化反应后的混合物中加入食盐可分离出高级脂肪酸钠,说明高级脂肪酸钠在 此时容易析出 |
C.等体积、 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说 都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性: 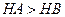 |
D.向浓度均为0.1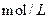 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成 的MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成 |
Cu(OH)2沉淀,说明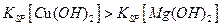
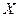 、
、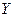 、
、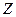 、
、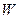 均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其它
均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其它
产物已略去):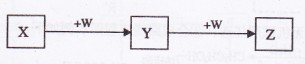
下列说法不正确的是
A.若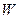 是单质铁,则 是单质铁,则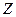 溶液可能是FeCl2溶液 溶液可能是FeCl2溶液 |
B.若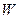 是氢氧化钠,则 是氢氧化钠,则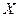 与 与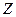 可反应生成 可反应生成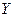 |
C.若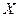 是金属镁,则 是金属镁,则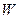 可能是强氧化性的单质 可能是强氧化性的单质 |
D.若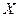 为甲醇,则 为甲醇,则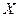 、 、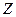 的相对分子质量可能相差14 的相对分子质量可能相差14 |
不定项选择题:本题包括6小题,每小题4分,共计24分。每小题有一个或两个选项符
合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,
只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
在下列各溶液中,离子一定能大量共存的是
A.能使酚酞试液变红的溶液中:Fe2+、Na+、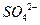 、 、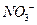 |
B.水电离出的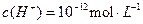 的溶液中:Na+、Ba2+、 的溶液中:Na+、Ba2+、 、 、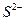 |
C.含有O.1 mol/L,Br一离子的溶液中: 、 、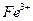 、 、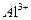 、 、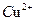 |
D.加入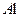 能放出氢气的溶液中: 能放出氢气的溶液中: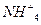 、 、 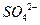 、 、 、CIO- 、CIO- |
下列有关化学实验不能达到目的的是
| A.采用如图所示的装置制取少量的氢氧化亚铁 |
| B.加热苯、液溴和浓硫酸的混合物制取少量的溴苯 |
| C.用素瓷片作催化剂进行石蜡油的受热分解实验 |
| D.用滴有少量硫酸铜溶液的稀硫酸跟锌粒反应快速地制氢气 |