在一容积固定的反应容器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下: A、 B和C均为4.0mol, D为 6.5mol, F为2.0mol,设E为xmol,x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中间位置。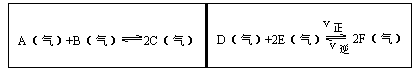
①若x=4.5,则右侧反应在起始时向______方向进行,欲使起始反应维持向该方向进行,则x的取值范围为____ 。
②若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等?______,其理由是______。
阅读下面的图表和短文,简要回答问题: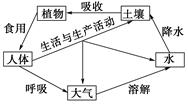
土壤污染是指土壤中积累有毒、有害物质,危害植物生长,或者残留在农作物中进入食物链而危害人体健康。人从自然界取得资源和能源,经过加工、调配和消费,最终以废弃物撒向土壤,或通过大气、水体和生物向土壤中排放和转移。当输入的污染物数量超过土壤的容量和自净能力时,必然引起土质的恶化,发生土壤污染。污染的土壤对农作物生长不利。
设计实验测定本地区土壤的酸碱性。(简要写出操作步骤)
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
据你所学化学知识提出防止土壤污染的措施。(至少3种)
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
我市某中学的同学自制一种黄色花汁,加入到不同试剂中,观察到的现象如下:
| 试剂 |
稀盐酸 |
食盐水 |
蒸馏水 |
草木灰水 |
石灰水 |
| 颜色 |
红 |
黄 |
黄 |
绿 |
绿 |
小强同学根据以上信息进行如下实验:
(1)用该花汁去检验附近小化工厂排放废水的酸碱性,显浅红色,则此废水显________性。
(2)用该花汁测知家中花盆土壤显酸性,打算加入上表中的____________________来改良。
用化学方程式表示用石膏、硫酸铝改良碱性土壤有关反应的离子(或化学)方程式____________________________、____________________________。
“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
SiO2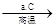 Si(粗)
Si(粗) 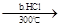 SiHCl3
SiHCl3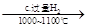 Si(纯)
Si(纯)
①写出步骤a的化学方程式_________________________________________________。
此反应不能证明C的非金属性比Si强,请你用一个化学方程式来说明C的非金属性比Si强的事实______________________________________。
②步骤b经过冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3的主要化学操作的名称是________;
(2)磁性材料。这种材料一般含有铁元素,铁以化学性质活泼用途广泛而著称。其中在工业上常用于印刷铜电路板工业,请写出反应的离子方程式_____________________________。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:__________________________________,________________________________。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直径大约是________,区分胶体和溶液最经典的方法是___________________。
(5)高分子材料。一种新型高效净水剂[AlFe(OH)nCl6-n]m属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为________价。
氧化铝有两种变体,一种是αAl2O3,一种是γAl2O3,γAl2O3可用Al(OH)3在723 K时加热制得,它不耐酸;αAl2O3是天然刚玉的主要成分,硬度很大,且对酸有极强的稳定性。αAl2O3可以用γAl2O3高温煅烧制得。已知氧化铝可由铝铵矾加热制得,铝铵矾[(NH4)Al(SO4)2·12H2O]受强热分解的产物为:Al2O3、NH3、N2、SO3、SO2和H2O。
(1)写出铝铵矾受强热分解的化学方程式_____________________________________
________________________________________________________________________,
氧化产物是________,还原产物是________,它们的物质的量之比为________。
(2)在含有1 mol的铝铵矾溶液中,需加入________molBa(OH)2,沉淀的物质的量最大,离子方程式为______________________________________________________________
________________________________________________________________________。
(3)将上述反应中的Al2O3加入适量的氧化铬,在氢氧焰上强热,熔融后使其结晶,可以制成人造红宝石,可用于做激光器材和装饰品。所得人造红宝石是哪种Al2O3的变体?________,如何用简单方法证明是该变体______________________________________
________________________________________________________________________。