对碱金属元素,随着核电荷数的增大,下列说法中正确的是( )
| A.原子半径依次增大,离子半径依次减小 |
| B.单质的熔点、沸点依次降低 |
| C.氧化物对应的水化物碱性依次增强 |
| D.单质的还原性依次减弱 |
下列有关实验操作或实验原理正确的是 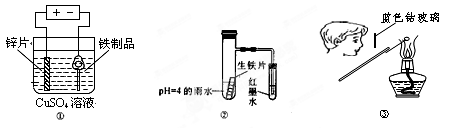
| A.用图①装置在铁制品表面镀锌 |
| B.用蒸发溶剂的方法,将10%的氯化铁溶液变为20%的氯化铁溶液 |
| C.用图②装置验证生铁片在pH=4的雨水中发生析氢还是吸氧腐蚀 |
| D.用图③装置检验K2CO3中的K+ |
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:
Pb+PbO2+2H2SO4 = 2PbSO4+2H2O,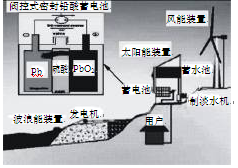
下列有关说法正确的是
| A.图中涉及的能量转化方式只有3种 |
| B.该发电工艺可实现零排放 |
| C.蓄电池供电时,负极的电极反应为:Pb-2e-=Pb2+ |
| D.储能时若充电时间过长,阳极流向阴极的 |
下列说法正确的是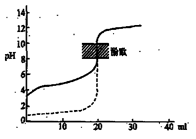
| A.△H>0的反应,常温下一定不能自发进行 |
| B.用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| C.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 |
D.恒容密闭容器中进行的反应3A(g) 2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变 2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变 |
下表所列各组物质中,不能通过一步反应实现如图所示转化的是
| 物质 选项 |
a |
b |
c |
| A. |
Cu |
CuSO4 |
CuO |
| B. |
Fe |
FeCl3 |
FeCl2 |
| C. |
AlCl3 |
Al(OH)3 |
NaAlO2 |
| D. |
Na2O2 |
Na2CO3 |
NaOH |
下列有关物质的性质或应用的说法中正确的是
| A.铝合金是一种混合物,它比纯铝的熔点高 |
| B.高炉中的主要反应是高温下焦炭和氧化铁直接作用炼出生铁 |
| C.铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜 |
| D.电解从海水中得到的氯化镁溶液可获得金属镁 |