(12分)“速力菲”是一种人工合成的补铁剂,某研究性学习小组为探究其主要成分,进行了如下实验:
(1)打开这种药片的密封膜,发现其外观为淡黄色。
(2)将“速力菲”投入小试管中,加入少量蒸馏水,充分振荡后发现溶液变浑浊;慢慢加入稀硫酸后溶液变得澄清透明并显黄色;滴加KSCN溶液,立即变为血红色。学生甲由此断定“速力菲”的主要成分是三价铁盐。
(3)学生乙的操作与甲大致相同,所不同的是他动作敏捷,且在振荡前用橡皮塞塞紧试管口。结果发现:溶液仅显示淡红色。乙同学认为“速力菲”的主要成分不是三价铁盐而是亚铁盐。
(4)为了确认甲、乙的结论是否正确,学生丙将乙所得的淡红色溶液分成两份继续进行实验:
试完成下列问题:
(1)甲、乙两位同学的结论中比较正确的是________,另一同学的结论不合理的原因是
________________________。
(2)丙的实验①说明维生素C具有较强的________性(填“氧化”或“还原”)。
(3)写出与②中现象对应的离子反应方程式________________________________。
(4)关于③中的实验现象,丙同学提出了两种假设:一种是过量的双氧水与Fe3+结合生成了某种稳定的新物质;另一种则是过量的双氧水将SCN-氧化了。请你设计一个实验方案以确认哪种假设更合理________________________________。
(5)针对实验目的,本次实验尚未完成的任务是__________________。
、某液态卤代烷RX(R是烷基,X是某种卤原子)的密度是a g·cm-3。RX可以与稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:
①准确量取该卤代烷bmL,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀硝酸酸化,滴加过量AgNO3溶液得到白色沉淀。
④将沉淀过滤、洗涤、干燥后称重,得到固体c g 。
回答下列问题:
(1)装置中长玻璃管的作用是。
(2)步骤④中洗涤的目的是为了除去沉淀吸附的离子。
(3)该卤代烷中所含卤素的名称是,判断依据是。
(4)该卤代烷的相对分子质量是(列出算式)。
(5)如果在步骤③中,加HNO3的量不足,没有将溶液酸化,则步骤④测得的c值 _________(填下列选项代码)。
| A.偏大 | B.偏小 | C.不变 | D.大小不定 |
实验室配制500mL 0.1mol/LNa2CO3溶液回答下列问题
(1)应用托盘天平称取十水碳酸钠晶体(Na2CO3·10H2O)_______g
(2)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的标号为____________
A.调整零点
B.将碳酸钠晶体放入小烧杯中称量
C.称量空的小烧杯
D.将砝码放回砝码盒内
E.记录称量结果
(3)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、_________ 、_________ 、_________ 。
(4)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时超过刻度线_________ ;
B.忘记将洗涤液转入容量瓶_________;
C.容量瓶内壁附有水珠而未干燥处理_________;
D.定容后摇匀液面低于刻度线_________ 。
E.转移时有少量液体溅出_________。
某实验需要100 mL、1 mol/L的Na2CO3溶液,现通过如下操作配制:
① 把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用(填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入(填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用(填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是(填序号)。
(2)若没有操作④,则所配溶液的浓度会(填“偏高”或“偏低”)。
(3)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为。
(4)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为mL
(5)在配制100 mL、1 mol/L的Na2CO3溶液时,下列操作中的会导致结果偏低(请用序号填写)
①用拖盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④定容时仰视刻度线
⑤干净的容量瓶未经干燥就用于配制溶液
现有某金属硝酸盐化学式为M(NO3)2,为了探究其热分解产物,某化学小组开展探究性学习:
[查阅资料]金属活泼性不同,其硝酸盐分解产物不同。如,2KNO3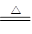 2KNO2+O2↑,
2KNO2+O2↑,
2Cu(NO3)2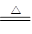 2CuO+2NO2↑+O2↑,4AgNO3
2CuO+2NO2↑+O2↑,4AgNO3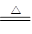 4Ag+4NO2↑+O2↑
4Ag+4NO2↑+O2↑
[提出猜想]猜想1 M(NO3)2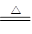 M(NO2)2+O2↑
M(NO2)2+O2↑
猜想2 2 M(NO3)2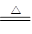 2MO+4NO2↑+O2↑
2MO+4NO2↑+O2↑
猜想3。
[设计实验]为了探究上述猜想,设计如下实验装置: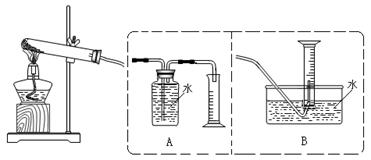
实验步骤:①连接仪器;②检查装置气密性;③取一定量样品装于大试管,并重新连接好仪器;④加热;⑤……
(1)写出猜想3的化学方程式:;
(2)测定气体体积应选择(填A或B);不选另一个装置的理由是;
(3)实验收集到一定量气体,为了检验收集气体的成分,其操作方法是;
(4)在实验后的水里加入适量碳酸氢钠粉末,溶液中产生大量气体,说明正确(填:猜想1.猜想2或猜想3);
(5)该小组测得两组数据:①实验前样品质量为Wg,收集到气体体积为V L;
②实验前样品质量为Wg,完全分解后测得固体产物质量为m g;
请你选择其中一组数据,计算M的相对原子质量为。
(本题共10分) 碱式碳酸铜【Cu2(OH)2CO3】是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
步骤一:废铜屑制硝酸铜:如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。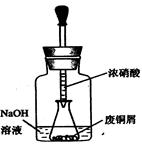
步骤二:碱式碳酸铜的制备:向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
①.上图装置中NaOH溶液的作用是_ _。反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有__ __(填写化学式)。
②步骤二中,水浴加热所需仪器有__ __、_ _(加热、夹持仪器、石棉网除外);
洗涤的目的是__ __。
③.步骤二的滤液中可能含有CO32-,写出检验CO32-的方法。
④.若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是____。