某温度下,在容积不变的密闭容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B、C的物质的量分别为4 mol、2 mol和4 mol。保持温度和容积不变,对平衡混合物中三者的物质的量做如下调整,A的转化率降低的是( )
2C(g)达到平衡时,A、B、C的物质的量分别为4 mol、2 mol和4 mol。保持温度和容积不变,对平衡混合物中三者的物质的量做如下调整,A的转化率降低的是( )
A.均加倍 B.加入1 mol C
C.均增加1 mol D.均减半
化学环境、材料、信息、能源关系密切,下列说法错误的是
| A.利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
| B.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| C.同时改变两个变量来研究反应速率的变化,不一定能更快得出有关规律 |
| D.防止酸雨发生的重要措施之一是使用清洁能源 |
设NA为阿伏加德罗常数。下列叙述不正确的是
| A.标准状况下,22.4 L O3含有分子的数目为NA |
| B.常温常压下,4.0 g CH4中含有共价键的数目为NA |
| C.常温常压下,1 L 0.1 mol/LNH4NO3溶液中NH4+、NO3-的数目均为0.1 NA |
| D.标准状况下,2.24 L Cl2与足量NaOH溶液反应,转移电子的数目为0.1 NA |
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是
| A.煤经过气化和液化等物理变化,可变为清洁能源 |
| B.服用铬含量超标的药用胶囊会对人体健康造成危害 |
| C.竹炭具有超强的吸附能力,能吸附新装修房屋内的有害气体 |
| D.采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 |
对下列装置的叙述错误的是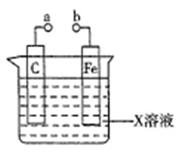
| A.X如果是HCl,则不论a和b用导线连接还是a和b分别连接直流电源正、负极时,H+的移动方向均相同 |
| B.X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加 |
| C.X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应 |
| D.X如果是NaCl,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程 |
在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g) △H<0,n(SO2)随时间的变化如表:
2SO3(g) △H<0,n(SO2)随时间的变化如表:
| 时间/min |
0 |
1 |
2 |
3 |
4 |
3 |
| n(SO2)/mol |
0.20 |
0.1 6 |
0.13 |
0.11 |
0.08 |
0.08 |
则下列说法正确的是
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4min内该反应的平均速率为0.005mol/(L·min)
C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大