在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g) △H<0,n(SO2)随时间的变化如表:
2SO3(g) △H<0,n(SO2)随时间的变化如表:
| 时间/min |
0 |
1 |
2 |
3 |
4 |
3 |
| n(SO2)/mol |
0.20 |
0.1 6 |
0.13 |
0.11 |
0.08 |
0.08 |
则下列说法正确的是
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4min内该反应的平均速率为0.005mol/(L·min)
C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
今有室温下四种溶液,有关叙述不正确的是 ( )
| ① |
② |
③ |
④ |
|
| pH |
11 |
11 |
3 |
3 |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH ①>②>④>③
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.VaL④与VbL②溶液混合后,若混合后溶液pH="4," 则Va ∶Vb= 11∶9
右图是温度和压强对X+Y 2Z反应影响的示意图。图中横坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中横坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
| A.上述可逆反应的正反应为放热反应 |
| B.X、Y、Z均为气态 |
| C.X和Y中只有一种为气态,Z为气态 |
| D.上述反应的逆反应的ΔH>0 |
下列说法正确的是
| A.可逆反应在其他条件不变时,升高温度,可以减小反应的活化能,加快反应速率 |
| B.S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表一个电子 |
| C.氮原子的第一电离能低于氧原子的第一电离能,因为氮比氧非金属性弱 |
| D.Fe3+比Fe2+稳定,因为Fe3+价电子构型是3d5,d亚层处于半充满状态,稳定 |
下列各组离子能在指定溶液中,大量共存的是:
①无色溶液中:K+,Cl—,Na+,H2PO4—,PO43—,SO42—
②使PH=11的溶液中:CO32—,Na+,AlO2—,NO3—,S2—,SO32—
③水电离的H+浓度C(H+)=10—12mol·L—1的溶液中:Cl—,HCO3—,NO3—,NH4+,S2O32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl—,K+,SO42—
⑤使甲基橙变红的溶液中:Fe3+,MnO4—,NO3—,Na+,SO42—
⑥酸性溶液中:Fe2+,Al3+,NO3—,I—,Cl—,S2—
| A.①②⑤ | B.①③⑥ | C.②④⑤ | D.②④ |
中学化学教材中,常借助于图像这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理。下列有关化学图像表现的内容错误的是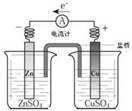
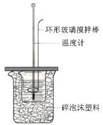
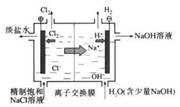

| A.铜锌原电池 | B.中和热测定装置 | C.离子交换膜法电解原理 | D.氨的制取装置 |