(6分)已知烯烃、炔烃在臭氧作用下发生以下反应:
CH3—CHCH—CH2—CH==CH2 CH3CHO+OHC—CH2—CHO+HCHO
CH3CHO+OHC—CH2—CHO+HCHO
CH3—C≡C—CH2—C≡CH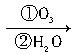 CH3COOH+HOOCCH2COOH+HCOOH
CH3COOH+HOOCCH2COOH+HCOOH
某烃化学式为C10H10,在臭氧作用下发生反应:
C10H10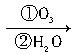 CH3COOH+3HOOC—CHO+CH3CHO
CH3COOH+3HOOC—CHO+CH3CHO
(1)C10H10分子中含_______________个双键,_______________个三键。
(2)C10H10结构简式为____________________________________________________________。
X、Y为两种主族元素,原子序数X小于Y,它们与元素Se三种元素原子序数之和为56。已知:X有两种氧化物M和N。Y与Se是相邻周期同主族元素,其中Se可以从电解精炼铜的阳极泥中获得。从阳极泥中提取Se的流程如下:
回答下列问题:(各元素用相应的元素符号表示)
⑴写出 X和Y形成的化合物的电子式。
X和Y形成的化合物的电子式。
⑵阳极泥中Se以单质、Ag2Se、Cu2Se等形式存在。写出①中Se单质与浓硫酸反
应的化学方程式

⑶写出反应②的化学方程式为。
⑷某温度下在容积固定的密闭容器中,下列反应达到平衡:
M(g)+H2O(g) N(g)+H2(g)
N(g)+H2(g)
| n(M):n(H2O) |
M转化率 |
H2O转化率 |
| 1:1 |
0.5 |
0.5 |
| 1:2 |
0.67 |
0.335 |
| 1:3 |
0.75 |
0.25 |
①已知M和H2的燃烧热分别为283kJ/mol、285.8kJ/mol,H2O(g)=H2O(l)△H=
—44kJ/mol,写出上述反应的热化学方程式。
②该反应的平衡常数为。该温度下,向容器中充入1molM、3mol H2O、
2mol N、1.5molH2,则起始时该反应速率V正V逆(填“>”、“<”或“=”)
③结合表中数据判断下列说法中正确的是
| A.增加H2O(g)的量,M的转化率升高而H2O(g)的转化率降低 |
| B.若M与H2O(g)的转化率相同时,二者的初始投入量一定相同 |
| C.M和H2O(g)初始物质的量之比等于二者转化率之比 |
| D.当M与H2O(g)物质的之比为1:4时,M的转化率为0.85 |
A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体。E、F、G、H、I为五种化合物,F不溶水,E为气体且极易溶于水成为无色溶液,G溶于水得棕黄色溶液。这九种物质间反应的转化关系如下图所示
(1)写出四种单质的化学式
A_________ B________ C_________D________
(2)写出E+F→H+I的离子方程式 ;
(3)写出G+I→H+D+E的化学反应方程式。
某有机物M是一种降脂药物,主要用于降低胆固醇,安全性好。其结构简式为: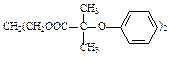 。M的合成路线如下。
。M的合成路线如下。
已知①E和F互为同分异构体,A属于芳香烃。
②CH3COOH BrCH2COOH
BrCH2COOH 。
。 请回答下列问题:
请回答下列问题:
(1)5.6 L(标准状况下)烃B在氧气中充分燃烧生成44 g CO2和18 g H2O,则B的分子式为____________。
(2)写出F的结构简式____________。J中含氧官能团的名称为______________。
(3)反应②的条件是__________。反应①~⑤中属于取代反应的有_________(填序号)。
(4)写出反应⑤的化学方程式__________________________________________。
(5)化合物L为I的同分异构体,若L既能与金属钠反应,又能发生银镜反应,则L可能的结构共有_____________种。
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下: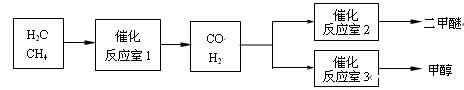
请填空:
(1)在一定条件下,反应室1(假设容积为10L)中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g),起始时按体积比1:2充入CH4和水蒸气,经过一段时间反应达到平衡状态,平衡时混合气的压强比起始时增大20%,则CH4的转化率为。
CO(g)+3H2(g),起始时按体积比1:2充入CH4和水蒸气,经过一段时间反应达到平衡状态,平衡时混合气的压强比起始时增大20%,则CH4的转化率为。
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为。
(3)在一定条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g) +2H2(g)  CH3OH(g) △H ,CO的平衡转化率与温度、压强的关系如图所示,则:
CH3OH(g) △H ,CO的平衡转化率与温度、压强的关系如图所示,则: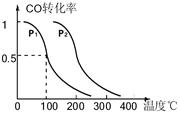
① P1P2 , △H_____0 (填“<”、“>”或“=”)。
②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率______(填“增大”、“减小”或“不变”) 。
③在P1压强下,100℃时,反应放出的热量为QkJ,则该条件下此反应的热化学方程式______________________________________。
A~F是中学常见物质,其中B、D、F均为单质,它们的相互转化关系如下图所示: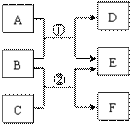
Ⅰ若A、C、E是氧化物,构成B、D的元素在同一主族,反应①②都是工业上的重要反应,通过反应②可以实现煤的气化,使煤变为清洁能源。
(1)写出反应①的化学方程式。
(2)用化学方程式表示E在冶金工业上的一种重要用途。
Ⅱ若A、C、E是氢化物,构成B和F的元素是第三周期的相邻元素,F是一种淡黄色固体,A能使湿润的红色石蕊试纸变蓝,A、E混合时有白烟生成。
(1)写出D的电子式。
(2)由A或C转化为E,每消耗1molB,转移电子的物质的量为mol。
(3)同温同压下,将V 1L A气体和V 2L E气体通入水中,
①若所得溶液的pH=7,则V1_____V2(填“>”或“<”或“=”)。
②若V1=2V2,反应后溶液中各离子浓度由大到小的顺序为。