根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
| A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等 |
| B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等 |
| C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等 |
| D.M层电子为奇数的所有主族元素所在族的序数与该元素原子M层电子数相等 |
下列热化学方程式书写正确的是(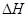 的绝对值均正确)
的绝对值均正确)
| A.S(s)+O2(g)===SO2(g);△H=—269.8kJ/mol(反应热) |
| B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
| C.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol(燃烧热) |
| D.2H2O==O2+2H2;△H=+571.6kJ/mol(反应热) |
关于如图所示装置的叙述,正确的是()。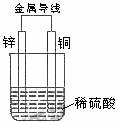
| A.氢离子在铜片表面被氧化 |
| B.铜片质量逐渐减少 |
| C.电子从锌片经导线流向铜片 |
| D.铜是阳极,铜片上有气泡产生 |
已知反应CO(g)=C(s)+1/2O2(g)的ΔH>0,ΔS<0。设ΔH 和ΔS 不随温度而变,下列说法中正确的是()。
| A.任何温度下都是非自发变化 |
| B.高温下是自发进行 |
| C.低温下是非自发变化,高温下是自发变化 |
| D.低温下是自发进行 |
对于可逆反应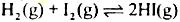 ,在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是
,在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是
| A.H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B.当体系的颜色不在发生改变时表明该反应已经达到平衡状态 |
| C.该正、逆反应速率的比值是恒定的 |
| D.达到平衡时,正、逆反应速率相等且都等于0 |
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。下列判断正确的是
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。下列判断正确的是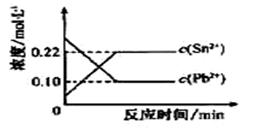
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变大 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=0.225. |