可用于合成下式代表的化合物的单体是( )
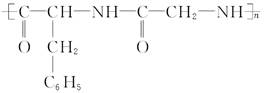
①氨基乙酸(甘氨酸) ②α-氨基丙酸(丙氨酸) ③α-氨基β-苯基丙酸(苯丙氨酸) ④α-氨基戊
二酸(谷氨酸)
| A.①③ | B.③④ | C.②③ | D.①② |
下列叙述中正确的是()
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、Hl的稳定性依次增强 |
| D.CS2、H2O、C2H2都是直线型分子 |
关于化学键的下列叙述中,正确的是()
| A.离子化合物中可能含有共价键 |
| B.共价化合物中可能含有离子键 |
| C.离子化合物中只含离子键 |
| D.共价键只能存在于化合物中 |
与NO3-互为等电子体的是( )
| A.SO3 | B.BF3 | C.CH4 | D.NO2 |
根据等电子原理:由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数
之和相同,可互称为等电子体,它们具有相似的结构特征。以下各组微粒结构不相似的()
| A.CO和N2 | B.O3和NO- | C.CO2和N2O | D.N2H4和C2H4 |
两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有 ( )
| A.1对 | B.2对 | C.3对 | D.4对 |