a mol  和b mol CH2==CH—CN加聚形成高聚物A,A
和b mol CH2==CH—CN加聚形成高聚物A,A
在适量氧气中恰好完全燃烧,生成CO2、H2O(g)、N2,在相同条件下,它们的体积比依次为12∶8∶1,则a∶b为( )
| A.1∶1 | B.3∶2 | C.2∶3 | D.1∶2 |
下列离子方程式正确的是
A.向NH4HSO3溶液中,加入过量的氢氧化钠溶液,并加热 NH4++OH- NH3↑+H2O NH3↑+H2O |
| B.向FeBr2溶液中通入过量氯气 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C.向次氯酸钠溶液中通入少量SO2气体 2ClO- + SO2 + H2O =" 2HClO" + SO32- |
D.实验室制氯气 MnO2 + 4H+ + 2Cl- Mn2+ + Cl2 ↑+2 H2O Mn2+ + Cl2 ↑+2 H2O |
向含下列离子的各组溶液中,分别加入Na2O2后,还能大量共存的一组是
| A.NH4+、Ca2+、NO3-、Cl- | B.K+、Mg2+、HCO3-、MnO4- |
| C.Na+、Ba2+、Cl-、I- | D.K+、Na+、CO32-、SO42- |
已知向某溶液中逐滴加入NaOH溶液时,测得生成沉淀的质量随所加入NaOH的体积变化如图所示,则该溶液中大量含有的离子可能是
| A.H+、NH4+、Al3+、NO3- | B.H+、Al3+、AlO2-、SO42- |
| C.H+、NH4+、Mg2+、Cl- | D.NH4+、Al3+、Cl-、SO42- |
如图所示等质量C2H6与X气体在相同温度下的密闭容器中,压强(P)与体积(V)的关系,则X气体可能是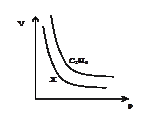
| A.H2 | B.NO | C.C2H2 | D.HCl |
已知一个12C的质量为 a g,一个18O的质量为b g,阿伏伽德罗常数的数值为NA,则下列说法中不正确的是
| A.18O的摩尔质量为:bNA g/mol | B.氧元素的相对原子质量: |
C.m g该氧原子的物质的量为: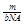 mol mol |
D.a= |