在苯的同系物中,加入少量高锰酸钾酸性溶液,振荡后溶液褪色,下列正确的解释是( )
| A.苯的同系物中碳原子数比苯分子中碳原子数多 |
| B.苯环被KMnO4所氧化而破坏 |
| C.侧链受苯环的影响而易被氧化 |
| D.苯环和侧链的相互影响,同时被氧化 |
根据金属活动性顺序,Ag不能发生反应:2HCl +2Ag =2AgCl+H2↑。但选择恰当电极材料和电解液进行电解,这个反应就能变为现实。下列四组电极和电解液中,为能实现该反应最恰当的是()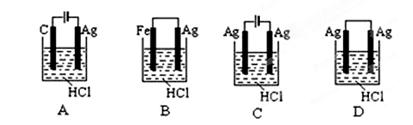
强酸与强碱的稀溶液发生中和反应的热效应为: H+(aq)+OH-(aq)===H2O(l) ΔH =-57.3kJ·mol-1。分别向1 L 0.5mol/L的NaOH溶液中加入①浓硫酸;②稀硫酸;③稀盐酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是( )
| A.ΔH1>ΔH2>ΔH3 | B.ΔH1<ΔH2<ΔH3 | C.ΔH1=ΔH2<ΔH3 | D.ΔH1<ΔH2=ΔH3 |
已知298K时下述反应的有关数据:C(s)+1/2 O2(g)=CO(g)△H1 = -110.5kJ·mol-1
C(s)+O2 (g)=CO2(g), △H2= -393.5kJ/mol则 C(s)+CO2(g)="2CO(g)" 的△H为
| A.283. kJ·mol-1 | B.+172.5 kJ·mol-1 |
| C.-172.5 kJ·mol-1 | D.-504 kJ·mol-1 |
用惰性电极电解下列溶液,起始时在阳极上不能生成O2的是()
| A.KNO3 | B.Na2S | C.Ba(OH)2 | D.H2SO4 |
已知:H(g) + H(g) = H2(g) ΔH=-435.7kJ/mol,此热化学方程式包含的意义是
| A.氢原子的能量比氢分子的能量低 |
| B.两个氢原子结合成一个氢分子时放出435.7kJ能量 |
| C.1mol氢分子分解成2mol氢原子要吸收435.7kJ能量 |
| D.2mol氢原子结合1mol氢分子成要吸收435.7kJ能量 |