科学家在不断深入的研究中,发现了一系列新的碳单质,对碳单质的研究现已发展成一门独立的学科——碳科学。1985年科学家发现的C60分子是由60个碳原子构成的,它的形状像足球(图C),因此又叫足球烯。1991年科学家又发现一种碳的单质——碳纳米管,它是由六边环形的碳原子构成的管状大分子(图D)。图A、B分别是金刚石和石墨的结构示意图。图中小黑点均代表碳原子。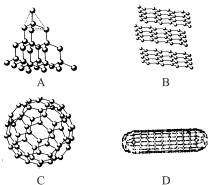
用你所学到的知识完成下列问题:
(1)碳纳米管由单层或多层石墨卷曲而成的,它是一种具有广阔发展前景的新型材料。关于碳纳米管的叙述不正确的是( )
A.不导电 B.充分燃烧生成二氧化碳
C.它和C60都是碳元素的同素异形体 D.它的性质和石墨的性质有相似之处
(2)金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是什么?
(3)常温下足球烯和碳纳米管的化学性质是否活泼?简要说明理由。
(4)请你设计一个方案,证明足球烯和碳纳米管都是由碳元素组成的。用文字简要叙述。
已知硫酸在水中的电离方程式是:H2SO4 = H+ + HSO4— HSO4— H++SO42—,回答下列问题:
H++SO42—,回答下列问题:
(1)Na2SO4溶液显 (填“酸性”,“中性”或“碱性”)。理由是(用离子方程式表示) 。
(2)在0.1 mol·L-1的Na2SO4溶液中,下列微粒浓度关系正确的有 。
| A.c(SO42—)+c(HSO4—)+c(H2SO4)="0.1" mol·L-1 |
| B.c(OH-)=c(H+)+c(HSO4—) |
| C.c(Na+)+c(H+)=c(OH-)+c(HSO4—)+2c(SO42—) |
| D.c(Na+)=2c(SO42—)+2c(HSO4—) |
(3)如果25 ℃时,0.1 mol·L-1的NaHSO4溶液中c(SO42—)="0.029" mol·L-1,则0.1 mol·L-1H2SO4溶液中c(SO42—) 0.029 mol·L-1(填“<”,“>”或“=”),理由是 。
(4)0.1 mol·L-1NaHSO4溶液中各种离子浓度由大到小的顺序是: 。
(5)如果25 ℃时,0.10 mol·L-1H2SO4溶液的pH="-lg" 0.11, 则25 ℃时,0.10 mol·L-1的H2SO4溶液中c(SO42—)= 。
向2 L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3——t4阶段为使用催化剂。观察下图,回答下列问题:
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为 。
(2)乙图中t2时引起平衡移动的条件是 ,t5时引起平衡移动的条件是 。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是 。
(4)该反应的化学方程式可以表示为: ,正反应为 (填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为 。
(1)在铝制易拉罐中收集一满罐CO2 ,加入过量浓NaOH溶液,立即把口封闭,可以发现易拉罐变瘪了;过了一会儿易拉罐又鼓起来了。请用离子方程式描述变化过程___________________________
(2)硅是现代信息材料重要的物质,写出工业上制取粗硅的方程式_________________
(3)写出制漂白粉的化学方程式: 。
Ⅰ、如果配制3mol/L的NaOH溶液500mL,需称量NaOH固体 g。
(1)在该溶液的配制过程中,用到的玻璃仪器: 、胶头滴管、量筒、烧杯、玻璃棒。
(2)如果在定容时仰视,溶液浓度将 ;若定容时液面高于刻度线应采取的措施是 。
Ⅱ、取上述实验中配制的NaOH溶液100mL,缓慢通入一定量的CO2,充分反应,测得最后溶液呈碱性。
(1)此时溶液的溶质若是单一成分,可能是 或 。
(2)若果在上述所得溶液中,逐滴缓慢滴加1mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑溶解于水)关系如图所示。
①由图可知,碱性溶液中的单一溶质为 。
②请写出0-A段所发生反应的离子方程式 。
③B点时,产生的CO2在标准状况下的体积为 mL;B点时,反应所得溶液中溶质的物质的量浓度是 mol/L(两种溶液混合时体积可以直接相加)。
(1)下列物质:①氯气、②铜片、③碳酸钙、④蔗糖、⑤HCl气体、⑥SO2气体、⑦氨水,能导电的是 ,属于电解质的是 。(填编号)
(2)现有:①铝、②二氧化硅、③二氧化硫、④二氧化碳、⑤三氧化二铁、⑥氢氧化钠、⑦氢氧化镁、⑧氢氧化铝、⑨氢氧化铁,能形成酸雨的是________;光纤制品的基本原料是__________;属于两性氢氧化物的是___________;红棕色固体是_____________。(填编号)
(3)节日焰火利用的是 反应,城市射灯在夜空形成五颜六色的光柱,属于 效应。
(4)胃舒平是治疗胃酸(盐酸)过多的常用药物。其中含有的有效成分是氢氧化铝,其治疗原理是(用化学方程式表示): ;碳酸氢钠也常用于治疗胃酸过多,写出反应的离子方程式 。