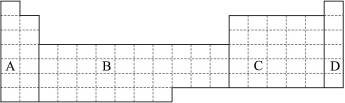
(1)在上面元素周期表中全部是金属元素的区域为____________。
a.A b.B c.C d.D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____________。
(3)现在甲、乙两种短周期元素,在室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素比较,金属性较强的是____________(填名称),可以验证该结构的实验是____________。
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别与同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
(10分)以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:
回答下列问题:
(1)写出氧化步骤中发生的主要反应的离子方程式。
(2)如何检验中和液中的杂质离子已完全除尽?。
(3)固体NH4Al(SO4)2·12H2O[相对分子质量:453]在加热时,固体残留率随温度的变化如图所示。
633℃时剩余固体的成分化学式为。
(4)综上分析,流程图中M的主要成分的化学式为,M可用一种物质吸收以实现循环利用,该物质的名称是。
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:
已知:反应Ⅱ包含2NaHSO3 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式:。
(2)“灼烧”时发生反应的化学方程式:。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:。
(4)副产品X的化学式是:;可循环利用的物质是:__________________。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为。
新型高效的甲醇燃料电池采用铂为电极材料,两电极上分别通入CH3OH和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
回答下列问题:
①甲醇燃料电池正极、负极的电极反应分别为___________________、_________________。
②闭合K开关后,a、b电极上均有气体产生,其中a电极上得到的是___________________,电解氯化钠溶液的总反应方程式为____________________________________________。
③若每个电池甲醇用量为3.2g,且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1列式计算),最多能产生的氯气体积为________L(标准状况)。
④若用该装置中的电解池精炼铜,在粗铜的电解过程中,粗铜板应是图中电极________(填“a”或“b”);在电极b上发生的电极反应式为____________________________________。
氯气在298 K、100 kPa时,在1 L水中可溶解0.09 mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的化学方程式为________________________________________________;
(2)估算该反应的平衡常数________________________________(列式计算);
(3)在上述平衡体系中加入少量NaCl固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将_______(填“增大”、“减小”或“不变”),平衡将向________移动。
(5)已知:H2CO3 HCO3-+ H+Ka1(H2CO3) = 4.45×10-7
HCO3-+ H+Ka1(H2CO3) = 4.45×10-7
HCO3- CO32-+ H+Ka2(H2CO3) = 5.61×10-11
CO32-+ H+Ka2(H2CO3) = 5.61×10-11
HClO H++ ClO-Ka(HClO) = 2.95×10-8
H++ ClO-Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;
(6)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是。
| A.MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力 |
| B.Mg与X2的反应是放热反应 |
| C.化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2 |
| D.MgF2(s)+Br2(l)===MgBr2(s)+F2(g) ΔH=+600 kJ·mol- 1 |
依上图数据写出 MgBr2(s)与 Cl2(g)反应的热化学方程式 。
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
(1)写出下列物质的化学式:D:____________,R:_______________;
写出下列物质的电子式A:;
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式:__________________;
B与R反应的化学方程式:___________________________ ;
D与盐酸反应的离子方程式:________________________。
(3)向沸水中加入W饱和溶液,可制得一种红褐色胶体,该反应的离子方程式为:_________。