实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取W g 该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按下图所示装置
进行实验:
回答下列有关问题:
(1)E装置的作用是___________________________________________________________。
(2)需要加热的装置是_________________________________________________________。
(3)写出氨基酸燃烧的方程式___________________________________________________。
(4)D的作用是_______________________________________________________________。
(5)F处读数时应注意的问题:_________________________________________________。
(6)还须测定的数据有_________________________________________________________。
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化。为了验证该结论,学生设计了如下图所示的实验装置进行实验(夹持装置略去)。圆底烧瓶A中的反应方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,请回答下列问题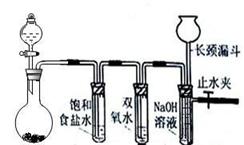
AB CD
(1)试管B中饱和食盐水的作用;
(2)试管C中加入5mL 30% 双氧水,发生反应的化学方程式____________________;
(3)试管D中充满10% NaOH溶液,NaOH溶液的作用是;
(4)将浓盐酸注入圆底烧瓶A,当装置中的空气基本排尽后关闭止水夹,反应一段时间后试管D中的现象为,试管D中的气体检验方法为__________________;
(5)有的同学对上述实验中试管D中气体来源产生质疑,你认为可能的来源有(用化学方程式表示),对于质疑可以采用对比实验来解决。
某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4 ·4H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
| 实验编号 |
初始 pH |
废水样品 体积/mL |
草酸溶液 体积/mL |
蒸馏水 体积/mL |
| ① |
4 |
10 |
30 |
|
| ② |
5 |
60 |
10 |
|
| ③ |
60 |
20 |
测得实验①和②溶液中的Cr2O72-浓度随时间变化关系如图所示。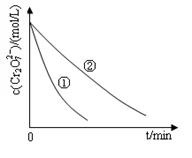
(2)实验①和②的结果表明_______________________________;
(3)该课题组队铁明矾[Al2Fe(SO4)4 ·4H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用;假设二:;假设三:;……
(4)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。(溶液中Cr2O72-的浓度可用仪器测定)
| 实验方案(不要求写具体操作过程) |
预期实验结果和结论 |
| 取_______________________________代替实验①中的铁明矾,控制其他反应条件与实验①相同,进行对比实验 |
反应进行相同时间后 若溶液中的Cr2O72-浓度____________________________则假设一成立; 若溶液中的Cr2O72-浓度____________________________则假设一不成立; |
下图是实验室制备四氯化硅的装置示意图。已知:四氯化硅遇水极易反应。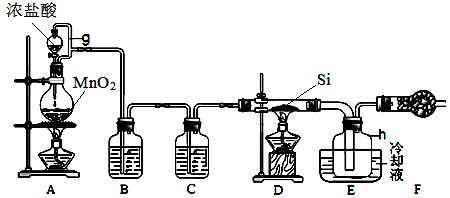
请回答下列问题:
(1)写出装置A中发生反应的化学方程式。
(2)装置A中g管的作用是。
干燥管F中碱石灰的作用是。
该组实验装置中存在的缺陷是。
已知①CH3CH2OH CH2=CH2↑+H20
CH2=CH2↑+H20
CH2=CH2+Br2 BrCH2—CH2Br
BrCH2—CH2Br
②乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示。
| 乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
| 通常状况下的状态 |
无色液体 |
无色液体 |
无色液体 |
| 密度/g·cm-3 |
0.79 |
2.2 |
0.71 |
| 熔点/℃ |
-130 |
9 |
-116 |
| 沸点/℃ |
78.5 |
132 |
34.6 |
某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。
(1)仪器E的名称是。
(2)仪器Ⅰ是漏斗,其左部的玻璃管的作用是(填字母)。
a.使漏斗中液体容易滴下
b.有利于吸收气体杂质
c.防止A中三颈烧瓶里的液体爆沸
(3)实验时,A中三颈烧瓶里放入几片碎瓷片的目的是。加热反应过程中,三颈烧瓶里除生成乙烯外,还可能生成的有机副产物主要是。
(4)反应过程中,若B中长玻璃导管(Ⅱ)里的液面上升,则说明可能是由于(填“D中出现堵塞”或“C中杂质已除尽”)造成的。
(5)反应过程中,D中需用冷水冷却盛有液溴的试管,其主要目的是。说明制备1,2-二溴乙烷的反应已经结束的实验现象是。
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大。小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+)。
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是。
(3)猜想Ⅱ可能是______________________________________________________________。要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是。
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
| 试管A |
试管B |
|
| 加入试剂 |
||
| (预期)实验现象 (褪色时间) |
||
| 结论 |
猜想Ⅱ正确 |