随着人们生活节奏的加快,方便的小包食品已被广泛接收。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
| A.无水硫酸铜、蔗糖 |
| B.硅胶、硫酸亚铁 |
| C.食盐、硫酸亚铁 |
| D.生石灰、食盐 |
下述实验不能达到预期实验目的的是
| 序号 |
实验内容 |
实验目的 |
| A |
室温下,使用pH计测定浓度均为0.1mol/L NaClO溶液CH3COONa |
比较HClO和CH3COOH的酸性强弱 |
| B |
向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 |
检验蔗糖水解产物具有还原性 |
| C |
向新生成的AgCl悬浊液中滴入KI溶液 |
研究沉淀的转化 |
| D |
室温下,向两支装有同体积同浓度过氧化氢溶液的试管中,分别加入3滴同浓度的氯化铜、氯化铁溶液 |
研究催化剂对反应速率的影响 |
组成和结构可用 表示的有机物共有(不考虑立体结构)
表示的有机物共有(不考虑立体结构)
| A.24种 | B.28种 | C.32种 | D.36种 |
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol/L Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是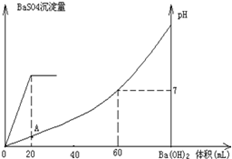
| A.图中A点溶液的pH=1 |
| B.生成沉淀的最大质量为2.33g |
| C.原混合溶液中盐酸物质的量浓度为0.1mol/L |
D.当 [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO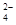 ═BaSO4↓ ═BaSO4↓ |
下列描述违背化学原理的是
| A.NaHCO3溶液与NaAlO2溶液混合产生白色沉淀,说明结合H+的能力:AlO2->CO32- |
| B.将SO2通入酸性高锰钾溶液中,溶液褪色,不能说明SO2具有漂白性 |
| C.高温时碳能置换出二氧化硅中的硅,说明还原性碳比硅强 |
| D.亚硫酸是良好的还原剂,浓H2SO4是良好的氧化剂,但两者混合,却不发生氧化还原反应 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2L正丁烷所含共用电子对数为7NA |
| B.常温常压下,5.6g乙烯与丁烯的混合物中含有氢原子的数目为0.8NA |
| C.在50g质量分数为56%的乙醇水溶液中,含有氢原子总数为3NA |
D.将CO2通过Na2O2使其增重a g时,反应中转移电子数为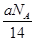 |