设X、Y、Z代表3种元素。已知:
①X+和Y-两种离子具有相同的电子层结构
②Z元素原子核内质子数比Y元素原子核内质子数少9个
③Y和Z两元素可以形成4核42个电子的负一价阴离子
据此,请填空:
(1)Y元素是_________,Z元素是_________。
(2)由X、Y、Z三元素所形成的含68个电子的盐类化合物的分子式(即化学式)是___________。
常温下,浓度均为0.1 mol/L的四种溶液:
①Na2CO3溶液 NaHCO3溶液③盐酸④氨水
试回答下列问题:
(1)上述溶液中有水解反应发生的是(填编号,下同),溶液中溶质存在电离平衡的是;
(2)比较①、②溶液,PH值较大的是;
(3)在溶液④中加入少量NH4Cl固体,此时 的值将(填“变小”,“变大”或“不变”);
的值将(填“变小”,“变大”或“不变”);
(4)用溶液③滴定V mL溶液④,其滴定曲线如右图所示:
①试分析在滴定过程中,滴定曲线上a、b、c、d四点:
水的电离程度最大的是点,理由是;
;
②a点溶液中离子浓度大小关系是;
③取少量c点溶液于试管,再滴加0.1 mol/L NaOH溶液至中性。此时溶液中除H+、OH-外,离子浓度大小关系是。
A、B、C、D、E、F六种短周期元 素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D 最外层电子数之比为2:3。试回答下列问题:
素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D 最外层电子数之比为2:3。试回答下列问题:
(1)A元素的名称是,E元素在周期表中的位置是;
(2)C、D、F的气态氢化物稳定性由强到弱的顺序是(填化学式);
(3)E单质在足量D单质中燃烧生成的化合物的电子式是;
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于化合物(填“离子”或“共价”);
②X与Y的水溶液相混合发生反应的离子方程式为;
(5)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为:。
回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下: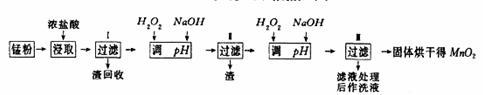
| 物质 |
开始沉淀 |
沉淀完全 |
| Fe(OH)3 |
2.7 |
3.7 |
| Fe(OH)2 |
7.6 |
9.6 |
| Fe(OH)2 |
8.3 |
9.8 |
(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式,该处理方法的缺点。
(2)步骤I中滤渣的化学式,步骤I中滤渣的化学式。
(3)向步骤I的滤液中加足量H2O2的作用为。再加NaOH溶液调节pH在3.7<pH<8.3,目的是。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起(填氧化剂、还原剂)的作用。
某有机物A可以通过不同的反应制得下列四种有机物: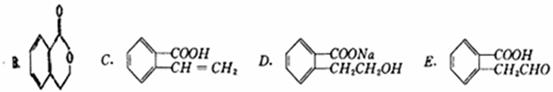
(1)A的结构简式为:,由A制取C的有机反应类型:;
(2)由A制B的化学方程式为:。
(3)B、C、D、E中互为同分异构体。
(4)A可以与反应生成D(写任意一种物质的化学式);
(5)有关B、C、D、E的叙述中正确的是。
A.四种有机物均为芳香烃
B.有机物E在加热时能与新制的氢氧化铜反应
C.1molB水解时最多可以消耗2molNaOH
D.1molC或E最多能与4molH2发生加成反应
附加题(1)石墨晶体的层状结 构,层内为平面正六边形结构(如图a),试回答下列问题:图中平均每个正六边形占有C原子数为____个、占有的碳碳键数为____个,碳原子数目与碳碳化学键数目之比为_______。
构,层内为平面正六边形结构(如图a),试回答下列问题:图中平均每个正六边形占有C原子数为____个、占有的碳碳键数为____个,碳原子数目与碳碳化学键数目之比为_______。
(2)2001年报道的硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如图 b所示的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内。则该化合物的化学式可表示为______
b所示的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内。则该化合物的化学式可表示为______ _。
_。