常温下,浓度均为0.1 mol/L的四种溶液:
①Na2CO3溶液 NaHCO3溶液 ③盐酸 ④氨水
试回答下列问题:
(1)上述溶液中有水解反应发生的是 (填编号,下同),溶液中溶质存在电离平衡的是 ;
(2)比较①、②溶液,PH值较大的是 ;
(3)在溶液④中加入少量NH4Cl固体,此时 的值将 (填“变小”,“变大”或“不变”);
的值将 (填“变小”,“变大”或“不变”);
(4)用溶液③滴定V mL溶液④,其滴定曲线如右图所示:
①试分析在滴定过程中,滴定曲线上a、b、c、d四点:
水的电离程度最大的是 点,理由是;
;
②a点溶液中离子浓度大小关系是 ;
③取少量c点溶液于试管,再滴加0.1 mol/L NaOH溶液至中性。此时溶液中除H+、OH-外,离子浓度大小关系是 。
在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。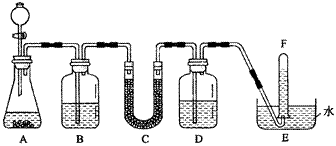
(1)A是用CaCO3制取CO2的装置。写出A中发生反应的化学方程式:
。
(2)按要求填写表中空格:
| 仪器编号 |
盛放的试剂 |
加入该试剂的目的 |
| B |
饱和NaHCO3溶液 |
|
| C |
与CO2反应,产生O2 |
|
| D |
吸收未反应的CO2气体 |
(3)为了达到实验目的,(填“需要”或“不需要”)在B装置之后增加一个吸收水蒸气的装置;若你认为需要增加一个吸收水蒸气装置,应选用作为吸水剂;若你认为不需要,请说明理由是。
(4)证明收集到的气体是氧气的方法是。
7分)某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下:(写出最佳答案)
(1)写出沉淀的化学式:沉淀1,白色沉淀2,
沉淀3;
(2)写出混合液加入A的离子方程式
(3)溶液加入B的离子方程式
已知:
| 溶解度 |
 |
C1- |
OH- |
| Ba2+ |
不溶 |
可溶 |
可溶 |
| Cu2+ |
可溶 |
可溶 |
不溶 |
| Ag+ |
微溶 |
不溶 |
不存在 |
在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。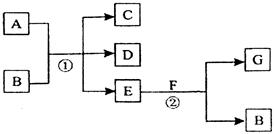
回答下列问题:
(1)A、G的化学式分别为___ ___、______。
(2)A和E反应的离子方程式为______。
(3)写出反应①的化学方程式,并用双线桥法表示出电子转移的情况______。
(4)在反应②中,每生成2.24 L气体G(标准状况)时,消耗F ____g。
已知X为Fe2O3和CuO的混合物,且知氧化性顺序:Fe3+>Cu2+>H+>Fe2+。取X样品进行如下图所示的实验: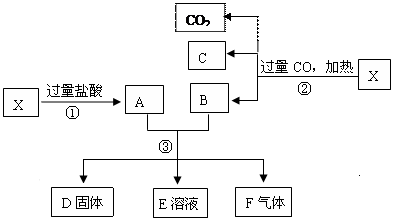
(1)写出③步可能发生反应的离子方程式为 。(共有3个)
(2)若溶液E中只有一种金属离子,则一定是;若溶液E含有两种金属离子,则一定是。
(3)若D固体是纯净物,该固体是。(填化学式)
(4)印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路的离子反应方程式为。
常温下,某未知酸性溶液中,可能含有大量的Cl-、OH-、CO32-、H+、Ag+、Fe3+ 等离子。你认为其中一定含有的离子是,一定不含有的离子是,还需进一步检验的离子是,为了进一步确认是否含该离子,需要的试剂和现象为。