在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
A.Na2O+H2O 2NaOH 2NaOH |
B.Mg3N2+6H2O 3Mg(OH)2↓+2NH3↑ 3Mg(OH)2↓+2NH3↑ |
| C.CaC2+2H2O→Ca(OH)2+CH≡CH↑ |
D.NH4Cl+NaOH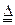 NaCl+NH3↑+H2O NaCl+NH3↑+H2O |
下列各组离子在溶液中能大量共存,加入OH-有沉淀生成,加入H+有气体生成的一组离子是
| A.K+、Mg2+、Cl-、HCO3- | B.K+、Cu2+、SO42-、Na+ |
| C.NH4+、CO32-、NO3-、Na+ | D.NH4+、Cl-、HCO3-、K+ |
下列离子检验的方法正确的是
A.某溶液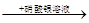 产生白色沉淀,说明原溶液中有Cl- 产生白色沉淀,说明原溶液中有Cl- |
B.某溶液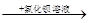 产生白色沉淀,说明原溶液中有SO42- 产生白色沉淀,说明原溶液中有SO42- |
C.某溶液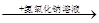 产生蓝色沉淀,说明原溶液中有Cu2+ 产生蓝色沉淀,说明原溶液中有Cu2+ |
D.某溶液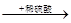 生成无色气体,说明原溶液中有CO32- 生成无色气体,说明原溶液中有CO32- |
分类是化学研究中常用的方法。下列分类方法中,正确的是
| A.根据元素原子最外层电子数的多少将元素分为金属和非金属 |
| B.依据组成元素的种类,将纯净物分为单质和化合物 |
| C.根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物和酸性氧化物 |
| D.根据分散系的稳定性大小,将分散系分为胶体、浊液和溶液 |
我国科学家通过测量SiO2中26Al和10Be两种元素的比例来确定“北京人”年龄,这种测量方法叫“铝铍测年法”。下列有关26Al和10Be的说法正确的是
| A.10Be和9Be是中子数不同质子数相同的同种核素 |
| B.10Be的原子核内质子数等于中子数 |
| C.5.2 g 26Al3+中所含的电子数约为1.2×1024 |
| D.26Al和26Mg的质子数和核外电子数均不同,中子数相同 |
下列说法不正确的是
| A.6.02×1023就是阿伏加德罗常数 |
| B.0.012 kg C12含有的碳原子数就是阿伏加德罗常数的值 |
| C.含有阿伏加德罗常数个粒子的物质的量是1 mol |
| D.1 mol NH3所含原子数约是2.408×1024 |