有一支50 mL酸式滴定管,其中盛有溶液,液面恰好在10.0 mL刻度处,把滴定管的溶液全部流下排出,盛接在量筒中,量筒内溶液的体积是()
| A.大于40.0 mL | B.大于10.0 mL | C.为40.0 mL | D.为10.0 mL |
下列物质是强电解质的是()
| A.CH3COOH | B.SO2 | C.BaSO4 | D.Cu |
关于水的离子积常数,下列说法不正确的是()
| A.Kw值随温度升高而增大 |
| B.纯水中,25℃时,c(H+)· c(OH-)=1×10-14 |
| C.25℃时,任何以水为溶剂的稀溶液中c(H+)· c(OH-)=1×10-14 |
| D.蒸馏水中,c(H+)· c(OH-)=1×10-14 |
下列各图所表示的反应是吸热反应的是()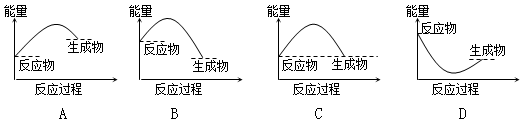
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g) zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断不正确的是 ()
zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断不正确的是 ()
| A.x+y﹥z | B.平衡向正反应方向移动 |
| C.B的转化率降低 | D.C的体积分数下降 |