(1)浓硫酸与木炭粉在加热条件下的化学方程式为_________________________。
(2)已知酸性KMnO4溶液可以吸收SO2,试用图4-6所示各装置设计一个实验,验证上述反应所产生的各种产物。
这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
__________→__________→__________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是______________________,B瓶溶液的作用是____________________,C瓶溶液的作用是_________________________。
(4)装置②中所加的固体药品是_______________,可确证的产物是_______,确定装置②在整套装置中位置的理由是_____________________。
(5)装置③中所盛溶液是__________,可验证的产物是__________。
右图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
(1)在圆底烧瓶中装入7—8 g的氢氧化钠、5 mL硬脂酸甘油酯,然后加入2—3 g的水和10 mL的酒精,加入酒精的作用是________________________________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成。向所得混合物中加入
_________________,静置一段时间,溶液分成上下两层,肥皂在_________________层,此操作名称为_________________。
(3)图中长玻璃管的作用是___________________________________________________。
(4)写出该反应的化学方程式:_______________________________________________。
为证明草本灰的主要成分是K2CO3,设计如下实验:
(1)提取碳酸钾晶体,可供选择的实验操作步骤有:
| A.过滤; | B.溶解; | C.浓缩结晶; | D.蒸发;E.冷却结晶;F.萃取;G.蒸馏。按照操作顺序,应选择___________(写编号),在实验中都要用到的仪器是___________。 |
(2)鉴定提取的晶体是碳酸钾______________________________________________。
我国北方人的生活和取暖多以煤为燃料。
(1)燃煤对生态环境有何危害?
(2)烟气中有大量煤粉,人们用静电除尘器来消除烟气中的煤粉,并回收利用。如图为静电除尘器的原理示意图。它由金属管A和悬挂在管中的金属丝B组成。A接电源正极,B接电源负极,在AB间产生很强的电场,且距B越近场强越大,试判断除尘器工作原理的正确说法是( )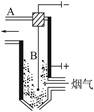
| A.烟气上升中,负极B使烟粉带负电,吸附到正极A上,在重力作用下,最后落入下边漏斗 |
| B.B极附近空气分子被电离,电子向正极运动过程中遇到煤粉使其带负电,吸附到正极A上,在重力作用下最后落入下边漏斗 |
| C.烟气上升中,煤粉在负极B附近被静电感应,使靠近正极A端带负电、引力较大,吸附到正极A上,在重力作用下最后落入下边漏斗 |
| D.烟气上升中,煤粉处在由A向B的强电场中被极化,在电场力作用下吸附到正极A上,在重力作用下,最后落入下边漏斗 |
(3)为了减少污染,提高利用率,现正兴起使用煤气,试用化学方程式表示其产生:_________________________
纯碱在日常生活和工业生产中用途广泛,需求量很大,因此纯碱的制备一直是科学家工作的一个重要方面。19世纪欧洲有个吕布兰制碱法,其主要反应原理是:
Na2SO4+2C Na2S+2CO2↑
Na2S+2CO2↑
Na2S+CaCO3====CaS+Na2CO3
这种方法的最大缺点是:①此反应是高温固体反应,不能连续生产;②浪费原料,CO2不能回收利用;③污染环境,CaS没有任何用处,只能抛至野外。由于这些缺点的存在和后来化学工业的发展,吕布兰法被索尔维法代替。索尔维法的生产流程如下:
索尔维法能实现连续生产,但其食盐利用率只有75%,且所得副产品CaCl2没有用处,污染环境。
我国化学家侯德榜经过一年的努力,做了500多次循环实验,终于设计出新的制碱工艺,于1943年11月在完成实验室规模的流程实验基础上,在工厂顺利试产,食盐的利用率达96%以上,得到了纯碱和氯化铵两种重要产品。氯化铵主要用作氮肥。侯德榜制碱法原理是:
①在30~50 ℃的饱和食盐水中,先通入氨至饱和,再通入二氧化碳得到碳酸氢钠沉淀;
②过滤,将滤渣加热而得到产品;
③滤液中加入细食盐末,在10~15 ℃,使NH4Cl沉淀,滤液为饱和食盐水。
据此回答下列问题:
(1)标出反应Na2SO4+2C Na2S+2CO2↑的电子转移方向和数目。
Na2S+2CO2↑的电子转移方向和数目。
(2)写出索尔维制碱法的各步反应的化学反应方程式:
①_________________________
②_________________________
③_________________________
④_________________________
(3)写出侯德榜制碱法第①步反应的化学方程式_________________________
(4)在索尔维制碱法中____________物质可循环利用。
(5)在侯德榜制碱法中____________物质可循环利用。
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀。两电极的材料分别为石墨和铁。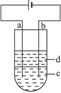
(1)a电极材料应为________________________________________,电极反应式为
_______________________________________________________;
(2)电解液c可以是(填编号)()
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为______________________________________________________,在加入苯之前对c应作怎样的简单处理?
______________________________________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施(填编号)()
A.改用稀硫酸作电解液
B.适当增大电源的电压
C.适当减少两电极间距离
D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为________________________________。