写出符合下列条件的元素原子的外围电子排布式:
(1)电负性最大的元素的原子______________。
(2)自然界中最活泼的金属元素的原子______________。
(3)第四周期0族元素的原子______________。
(4)能形成自然界中最硬的单质的元素原子______________。
生活中常用药品很多,如:①碘酒、②麻黄碱、③青霉素、④阿司匹林、⑤葡萄糖注射液、⑥胃舒平(含氢氧化铝、淀粉等)。
(1)上述物质中属于抗生素的是_____(填写序号,下同),具有止咳平喘作用的天然药物是 。
胃舒平可防治胃酸分泌过多,其发挥功效时的离子方程式为 。
(2)低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是_________(填写字母,下同)。
| A.加成反应 | B.取代反应 | C.氧化反应 | D.聚合反应 |
(共11分)拆开1mol H—H键,1mol N—H键,1mol N三N键分别需要吸收的能量为436kJ ,391kJ,946kJ(计算结果保留到整数)
写出此反应的热化学方程式(此空5分)
则1mol N2 完全生成NH3热量(填:吸收或放出) kJ;
1mol H2完全生成NH3 热量(填:吸收或放出) kJ;
理论上,完全分解1mol NH3热量(填:吸收或放出) kJ
将33.6L(标况下)乙烯和甲烷混合气体,通入足量的溴水中,充分反应后,水溶液的质量增加了14g。则原混合气体中乙烯与甲烷的体积之比为
写出下列化学方程式(共6分)
(1) 乙炔与氯化氢按物质的量比1:1反应
(2) 苯与浓硝酸、浓硫酸的混合酸共热__________
下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合(氢原子省略)。回答下列问题: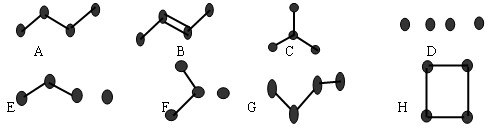
(1)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可
以形成 和 ,还可以形成碳环。
(2)图中属于烯烃的是(填编号)
(3)与A 互为同分异构体的是(填编号)
( 4) 写出上图中B、C、G的结构简式
B 、C 、G .