金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以,和金属离子的配离子的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和,在<2的条件下加热蒸馏,蒸出所有的,并用溶液吸收。
②滴定:将吸收液调节至>11,以试银灵作指示剂,用标准溶液滴定
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
(1)水样预处理的目的是。
(2)水样预处理的装置如右图,细导管插入吸收液中是为了。

(3)蒸馏瓶比吸收液面要高出很多,其目的是。
(4)如果用盐酸代替磷酸进行预处理,实验结果将(填"偏高"、"无影响"或"偏低")。
(5)准确移取某工厂污水100,经处理后用浓度为0.01000的硝酸银标准溶液滴定,终点时消耗了21.00。此水样中含氰化合物的含量为(以计,计算结果保留一位小数)。
资料显示:在一定条件下黄铵铁钒在pH=0.5~2.5范围内均能稳定存在,工业上用酸浸法制取硫酸铜的流程示意图如下: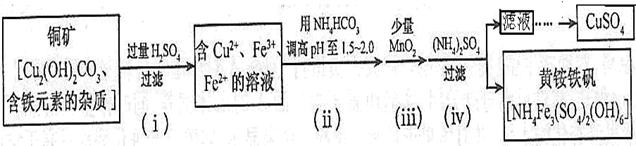
根据题意完成下列问题:
(1)步骤(ii)所加试剂起调节pH作用的离子是 (填离子符号)。
(2)在步骤(iii)发生的反应中,加入少量MnO2的作用是
(3)步骤(iv)除去杂质的离子方程式可表示为
(4)实验室模拟碱式碳酸铜[Cu2(OH)2CO3]的制备,向大试管中加入碳酸钠溶液和硫酸铜溶液,水浴加热至70℃左右,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。根据上述碱式碳酸铜的制备方法,请完成以下问题:
①过滤后洗涤的目的是什么;简述如何洗涤沉淀
②若实验得到a g样品(只含CuO杂质),取此样品加热至分解完全后,得到b g固体,此样品中碱式碳酸铜的质量分数是
重铬酸钠(Na2Cr2O7·2H2O)俗称红矾钠,是一种重要的无机盐产品,可作氧化剂,在印染、颜料、电镀、医药等工业方面有广泛的用途。某化学兴趣小组设计实验测定市场上的红矾钠中Na2Cr2O7的质量分数,其步骤如下:
I.称取Wg红矾钠,溶于酸配成l00mL溶液;
Ⅱ.用cmol·L-1的标准KMnO4酸性溶液滴定20.00mL一定浓度的FeSO4溶液,消耗KMnO4溶液20.00rnL;
Ⅲ。取20.00mL Na2Cr2O7溶液,用上述FeSO4溶液滴定,达到滴定终点时,消耗24.00mLFeSO4溶液;
查阅资料知:Cr2O72-在酸性条件下具有强氧化性,易被还原为Cr3+
回答下列问题:
(1)Na2Cr2O7与FeSO4的反应离子方程式为.
(2)步骤Ⅱ中的滴定过程,滴定终点的现象为;选用(填“酸式”或“碱式”)滴定管。
(3)已知:MnO4-+5Fe2++8H+==Mn2++5Fe3++4H2O,此红矾钠中Na2Cr2O7的质量分数的表达式为。
(4)判断下列操作对Na2Cr2O7的质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”):
①步骤Ⅲ中的滴定过程,滴定终点读数时俯视读数;
②配制c mol·L-1的KMnO4标准溶液时,转移时有少量溶液洒出。
(5)[实验探究]有同学提出FeSO4有很强的还原性,在空气中易被氧化而变质,因此对测定结果会造成影响,请你分析后指出,如果FeSO4变质,对测定结果的影响是(填“偏高”、“偏低”或“无影响”)。
请设计一个简单实验检验FeSO4溶液是否变质。
乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答: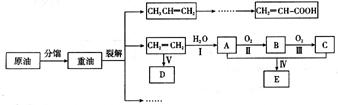
已知: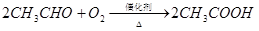
(1)反应II的化学方程式是。
(2)D为高分子化合物,可以用来制造多种包装材料,其结构简式是。
(3)E是有香味的物质,在实验室用下图装置制取。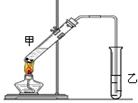
①反应IV的化学方程式是,该反应类型为。
②该装置图中有一个明显的错误是。
(4)为了证明浓硫酸在反应IV中起到了催化剂和吸水剂的作用,某同学利用上图改进后装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
| 实验编号 |
试管甲中试剂 |
试管乙中试剂 |
有机层的厚度/cm |
| A |
2 mL乙醇、1 mL乙酸、 1mL18mol·L-1浓硫酸 |
饱和Na2CO3溶液 |
3.0 |
| B |
2 mL乙醇、1 mL乙酸 |
0.1 |
|
| C |
2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 |
0.6 |
|
| D |
2 mL乙醇、1 mL乙酸、盐酸 |
0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是3mL和mol·L-1。
②分析实验(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有和。
(2)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法是:在100ml稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况):
| 时间/min |
1 |
2 |
3 |
4 |
5 |
| 体积/mL |
50 |
120 |
232 |
290 |
310 |
①哪一时间段反应速率最大(填“0~1 min”或“1~2 min”或“2~3 min”或“3~4 min”或“4~5min”)。
②2~3 min时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)为。
③试分析1~3min时间段里,反应速率变大的主要原因。
1,2-二溴乙烷在常温下是无色液体,密度是2.18g/cm ,沸点是131.4℃,熔点是9.79℃,不溶于水,易溶于醇、丙酮等有机溶剂。在实验室中可以用下图所示装置来制备1,2-二溴乙烷。其中试管c中装有液溴(表面覆盖少量水)。
,沸点是131.4℃,熔点是9.79℃,不溶于水,易溶于醇、丙酮等有机溶剂。在实验室中可以用下图所示装置来制备1,2-二溴乙烷。其中试管c中装有液溴(表面覆盖少量水)。
(1)写出制备1,2-二溴乙烷的化学方程式________。
(2)安全瓶a可以防止倒吸,并可以检查实验进行时试管c中导管是否发生堵塞。如果发生堵塞,a中的现象是__________。
(3)容器b中NaOH溶液的作用是__________,容器d中NaOH溶液的作用是__________。
(4)试管c浸入冷水中,以及液溴表面覆盖少量水的原因是__________。
(5)某同学在做实验时,使用一定量的液溴,当溴全部褪色时,通入的乙烯混合气体的量比正常情况下超出许多。如果装置的气密性没有问题,试分析可能的原因________________.