、、三者均为短周期元素,已知元素有一种同位素不含中子,元素原子的最外层电子数是次外层电子数的2倍,元素原子的最外层电子数是次外层电子数的3倍。下列化学式①、②、③、④、⑤、⑥中,并非都存在的一组分子是()
| A. | ①② | B. | ④⑥ | C. | ③⑤ | D. | ②④ |
下列反应属于吸热反应的是()
A.C6H12O6(葡 萄糖)+6O2→6CO2+6H2O 萄糖)+6O2→6CO2+6H2O |
| B.HCl+KOH="===" KCl+H2O |
| C.反应物的总能量大于生成物的总能量 |
| D.破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量 |
由于碘是卤素 中原子半径较大的元素,可能呈现金属性。下列事实能够支持这个结论的是( )
中原子半径较大的元素,可能呈现金属性。下列事实能够支持这个结论的是( )
| A.已经制得了I2O5等碘的氧化物 |
| B.在IBr、ICl等卤素互化物中碘元素表现正价 |
| C.已经制得了I(NO3)3、I(ClO4)3·2H2O等离子化合物 |
| D.碘(I2)易溶于KI等碘化物的溶液,形成I |
 是一种高效多功能水处理剂。一种制备
是一种高效多功能水处理剂。一种制备 的方法可用化学方程式表示如下:
的方法可用化学方程式表示如下: 

 ↑,下列说法中不正确的是()
↑,下列说法中不正确的是()
A. 在上述反应中只作氧化剂 在上述反应中只作氧化剂 |
B. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
C. 处理水时,既能杀菌,又能在处理水时产生胶体净水 处理水时,既能杀菌,又能在处理水时产生胶体净水 |
D.2 mol  发生反应时,共有10 mol电子发生转移 发生反应时,共有10 mol电子发生转移 |
下列说法正确的是 ( )
| A.高纯度的二氧化硅可用于制造计算机芯片和太阳能电池 |
| B.胶体和溶液可以通过滤纸进行分离 |
| C.雾是气溶胶,在阳光下可观察到丁达尔效应 |
| D.玻璃是氧化物,成分可表示为Na2O·CaO·6SiO2 |
已知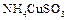 与足量的10 mol/L硫酸混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色据此判断下列说法正确的是()
与足量的10 mol/L硫酸混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色据此判断下列说法正确的是()
| A.反应中硫酸作氧化剂 |
B.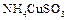 中硫元素被氧化 中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
D.1 mol 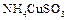 完全反应转移0.5 mol电子 完全反应转移0.5 mol电子 |