人的纯净的胃液是一种强酸性液体,pH在0.9~1.5之间,氢氧化铝是一种治疗胃液过多的胃药的主要成分.目前这种胃药已不常用,原因主要是( )
| A.长期摄入铝元素不利于人体健康 |
| B.它不能中和胃液 |
| C.它不易溶于胃液 |
| D.它的疗效太差 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=1的溶液中:Ca2+、Fe2+、NO3-、CO32- |
| B.Kw/c(OH-)="0.1" mol•L-1的溶液中:Na+、NH4+、Cl-、NO3- |
| C.c(Fe3+)="0.1" mol•L-1的溶液中:K+、SCN-、SO42-、Cl- |
| D.由水电离的c(H+)=1×10-14 mol•L-1的溶液中:Na+、AlO2-、HCO3-、OH- |
化学用语是学习化学的工具和基础。下列有关化学用语的表达正确的是
| A.质量数为37的氯原子:1737Cl |
B.Al(OH)3的电离方程式:H++AlO2-+H2O Al(OH)3 Al(OH)3 Al3++3OH- Al3++3OH- |
| C.CO2的结构式:O=C=O |
D.次氯酸分子的电子式: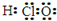 |
下列用品的主要成分及其用途对应不正确的是
| A |
B |
C |
D |
|
| 用品 |
铁罐车 |
 |
 |
 |
| 主要成分 |
Fe |
NaHCO3 |
Si |
Fe2O3 |
| 用途 |
可运输浓硫酸 |
发酵 |
光导纤维 |
涂料 |
一定条件下合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是:
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是:
| A.生成乙烯的速率:v(M)有可能小于v(N) |
| B.平衡常数:KM>KN |
| C.当温度高于250℃,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低 |
| D.若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7% |
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是:
A.某HCl溶液的pH值为2,则溶液中由水电离的c(H+)=10-2mol•L-1
B.0.1 mol•L-1的KHA溶液,其pH=10, c(K+)>c(A2-)>c(HA-)>c(OH-)
C.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D.将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后溶液pH>7,则反应后的混合液:c(HA)>C(Na+)>c(A-)