研究性学习小组进行SO2的制备及性质探究实验。
(1)根据反应Na2SO3(g)+H2SO4(浓)====Na2SO4+SO2↑+H2O,制备SO2气体。
(2)有一小组在实验中发现,SO2产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。
请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因:____________________,
验证方法:________________________________________。
②原因:____________________,
验证方法:________________________________________。
③原因:____________________,
验证方法:________________________________________。
用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象可得出两条有关过氧化钠跟水反应的结论是:第一:有氧气生成;
第二:____________________。
(2)某研究性学习小组拟用如下图所示的装置进行实验,以验证上述结论。用以验证第一条结论的实验操作_______________ ,现象是______________________。
为了验证第二条结论,将管口b浸入水中,可观察到的现象为_____________。
(28分)
[1]由碳、氢、氧三种元素组成的某有机物分子中共含有13个原子,其原子核外共有40个电子,l mol该有机物在氧气中完全燃烧时需消耗5.5 mol O2。请回答:
(1)试求出该有机物的分子式为 。
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,取0.1 m ol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是 ;该有机物在一定条件下发生聚合反应的化学方程式是 。
ol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是 ;该有机物在一定条件下发生聚合反应的化学方程式是 。
(3)若该有机物能发生银镜反应,且分子中只含有一个甲基,则其结构简式是 。
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其键线式是 。
|
[2]2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。“亮菌甲素”的结构简式为,它配以辅料丙二
|
醇

在75℃左右,实验室用HgSO4做催化剂,可使乙炔与水反应制取乙醛。装置图如下:(夹持装置均已略去)
供选用试剂:电石(混有CaS等杂质)、HgO粉末、浓H2SO4、NaOH溶液、蒸馏水
资料提示:CaS遇水会产生H2S气体;HgSO4遇到H2S会发生催化剂中毒而失去活性。
回答下列问题:
(1)加入药品前,必须对装置进行的操作是:。
(2)装置B中盛放的试剂为 ,作用是
(3)写出A中发生的主要反应的化学方程式
(4)反应温度应控制在75℃左右,采用E装置的优点是
有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些认识,某教师设计了如图装置(夹持装置仪器已省略),其实验操作为:先按图安装好,先关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)通入气体,即可在M处观察到明显的实验现象。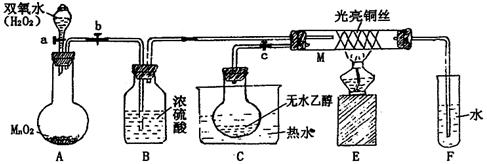
(1)A中发生反应的化学方程式:_______________________________ ,
B的作用:________________________;
(2)M处发生的反应的化学方程式为:______________________________________
(3)该实验过程中催化剂______________ (填“参加”或“不参加”)了化学反应
(4)实验乙醇氧化产物的试剂是,并写出对应的化学方程式
。
(5)若试管F中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含
有。要除去该物质,可现在混合液中加入(填写字母)。
| A.氯化钠溶液 | B.苯 | C.碳酸氢钠溶液 | D.四氯化碳 |
已知乙醇可以和无水CaCl2反应生成微溶于水的CaCl2•6C2H5OH 。
有关试剂的沸点如下:CH3COOC2H577.1℃; C2H5OC2H534.5℃;
C2H5OH 78.3℃; CH3COOH 118℃。
某课外小组用如下图所示装置制备乙酸乙酯粗产品,试回答下列问题:
(1)蒸馏烧瓶中加入的试剂是:冰乙酸、酒精和浓硫酸,
其中浓H2SO4的作用是和。
(2)冷凝管中最先冷凝的馏分是,弃去低沸点的馏分。收集沸点在76℃~120℃
之间的馏分,将其倾倒入饱和Na2CO3溶液中观察到的现象是:。
上述实验中饱和碳酸钠溶液的作用是_____(填序号)
A.中和乙酸和乙醇;B.中和乙酸并溶解乙醇;
C.加速酯的生成,提高酯的产率 D.有利于分层析出。
(3)写出上述实验中用CH3COOH、CH3CH218OH和浓硫酸制备乙酸乙酯的化学方程式:
。
(4)分离出粗产品乙酸乙酯,再加入无水CaCl2,震荡分离的目的是:
为了干燥乙酸乙酯可选用的最佳干燥剂为 ________(填序号)
A.五氧化二磷 B.无水硫酸钠 C.碱石灰 D.固体氢氧化钠