物质的制备方法可以分为实验室制法和工业制法。下列反应中既属于氧化还原反应又属于实验室制法的是
①制SO2:Na2S2O3+H2SO4 ="===" Na2SO4+H2O+SO2↑+S↓
②制氧气: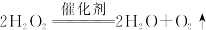
③制氯气: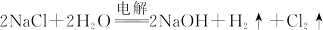
④制氨气: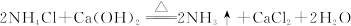
⑤制硝酸: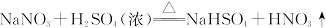
⑥制H2:Mg+H2SO4====MgSO4+H2↑
| A.①②③⑥ |
| B.② |
| C.②⑥ |
| D.全部 |
下列各组粒子不能互称为等电子体的是:
| A.CO和N2 | B.O3和SO2 | C.CO2和N2O | D.N2H4和 C2H4 |
在常温常压下呈气态的化合物,降温固化得到的晶体属于:
| A.原子晶体 | B.分子晶体 | C.离子晶体 | D.金属晶体 |
以下能级符号正确的是:
| A.1p | B.2d | C.3f | D.4s |
对SO2与CO2说法正确的是()
| A.都是直线形结构 | B.中心原子都采取sp杂化轨道 |
| C.S原子和C原子上都没有孤对电子 | D.SO2为V形结构, CO2为直线形结构 |
在pH=1的无色为溶液中,能大量共存的离子组是( )
| A.NH4+、Mg2+、SO42-、Cl- |
| B.Ba2+、K+、OH-、Cl- |
| C.Al3+、MnO4-、SO42-、Cl- |
| D.Na+、Cu2+、Cl-、Ba2+ |