煤燃烧的反应热可通过以下两个途径来利用:A.利用煤在充足的空气中直接燃烧产生的反应热;B.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)====CO2(g) ΔH=E1①
b.C(s)+H2O(g)====H2(g)+CO(g) ΔH=E2②
H2(g)+1/2O2(g)====H2O(g) ΔH=E3③
CO(g)+1/2O2(g)====CO2(g) ΔH=E4④
完成下列问题:
(1)与途径a相比途径b有较多的优点,即_________________________。
(2)上述四个热化学方程式中的哪个反应的ΔH>0?___________________。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用总能量关系正确的是________。
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为_________________________。
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
(1)由图中信息可知HA为________酸(填“强”或“弱”),理由是____________
(2)常温下一定浓度的MA稀溶液的pH=a,则a________7(填“>”、“<”或“=”),用离子方程式表示其原因为__________________________;,此时,溶液中由水电离出的c(OH-)=________。
(3)请写出K点所对应的溶液中离子浓度的大小关系:__________
(4)K点对应的溶液中,c(M+)+c(MOH)________2c(A-)(填“>”、“<”或“=”);若此时溶液中,pH=10,则c(MOH)+c(OH-)=________mol·L-1。
A、F、G是单质,其中A、F是金属单质,且A是现在用途最广用量最大的金属。F具有黄色的焰色反应,G是黄绿色气体;B、C、D、E是化合物;E到D的现象为白色沉淀变为灰绿色,最后变为红褐色,它们之间存在如下图所示的转化关系(生成物没有全部写出):
(1)推断:A__________F_______(填化学式)
(2)写出E→D的化学方程式____________。
(3)写出C→B的离子方程式________________________。
硅和硅的化合物既是传统的无机非金属材料又是重要的现在新型材料。
(1)陶瓷、玻璃、水泥的组成中的共同成分是__________盐。
(2)2009年,华裔科学家高锟以研究传播力纤维光信号传输的骄傲成绩获得诺贝尔物理奖,制造光导纤维的原材料是______________。
新制氯水中含有Cl2、H2O、HClO、H+、Cl-等粒子,根据下列性质选择恰当的粒子进行填空。
①使新制绿水呈现浅黄绿色的物质是___________________.
②能起杀菌消毒作用,光照易分解的弱酸是______________.
③能与硝酸银作用生成白色沉淀的离子是_______________.
(10分)下表列出了①~⑥六种元素在元素周期表中的位置。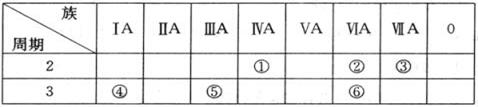
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是____(填写元素符号);
(2)元素①③⑥的氢化物的化学式分别是__ __;___ _;__ _ _.
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是______ ____________。