X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
| A.33% | B.40% | C.50% | D.65% |
萃取碘水中的碘,可选取的萃取剂是
①四氯化碳;②汽油;③酒精
| A.只有① | B.①和② | C.①和③ | D.①②③ |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是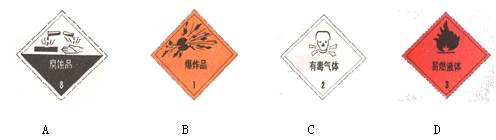
下列说法不正确的是
| A.在标准状况下,0.5molO2和0.5molN2组成的混合气体体积约为22.4L |
| B.在标准状况下,1mol任何气体的体积都约为22.4L |
| C.1molH2的质量只有在标准状况下才约为2g |
| D.273℃,101×105Pa状态下,1mol气体体积大于22.4L |
如果你家里的食用花生油混有水份,你将采用下列何种方法分离
| A.过滤 | B.蒸馏 | C.分液 | D.萃取[ |
下列说法中,正确的是
A.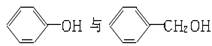 互为同系物 互为同系物 |
| B.乙醇和乙醚互为同分异构体 |
| C.乙醇、乙二醇、丙三醇互为同系物 |
| D.可用浓溴水来区分乙醇和苯酚 |