下列反应的离子方程式正确的是 
A.硫化钠的水解反应:S2-+H3O+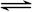 HS-+H2O HS-+H2O |
| B.用铜做阳极电解氯化铜溶液:Cu2++2Cl-Cu+Cl2↑ |
| C.在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O |
| D.在氢氧化钡溶液中滴加硫酸氢钾溶液至pH=7:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 叙述I |
叙述II |
|
| A |
水玻璃具有黏性 |
盛装烧碱溶液的试剂瓶不能用玻璃塞 |
| B |
往氯化钙溶液中通入足量的CO2 先有白色沉淀生成,后沉淀溶解 |
CaCO3不溶于水,Ca(HCO3)2可溶于水 |
| C |
NH4Cl受热易分解 |
可用加热法除去I2中的NH4Cl |
| D |
利用丁达尔现象区分氢氧化铁胶体和浓的氯化铁溶液 |
往氢氧化钠溶液中滴加饱和氯化铁溶液,加热至红褐色制得胶体 |
用NA表示阿伏加德罗常数,下列说法中正确的有
| A.pH=13的NaOH溶液中含有的OH-的数为0.1 NA |
| B.Fe在少量Cl2中燃烧生成0.5 mol 产物,转移的电子数为1 NA |
| C.18g D2O中含有的质子数为9NA |
| D.标准状况下,含4 mol HCl的浓盐酸与足量MnO2加热反应可生成22.4 L氯气 |
常温,下列各组离子一定能大量共存的是
| A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B.在透明溶液中:Na+、Cu2+、SO42-、NO3- |
| C.在c(H+)=10-13 mol/L的溶液中:NH4+、Al3+、SO42-、CO32- |
| D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
下列说法正确的是
| A.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可以发生水解反应 |
| B.煤经气化和液化两个物理变化过程,可变为清洁能源 |
| C.聚酯纤维、有机玻璃、光导纤维都属于有机高分子材料 |
| D.植物油和裂化汽油都能使溴水褪色 |
下列实验操作、现象和解释都正确的是
| 选项 |
实验操作 |
现象 |
解释 |
| A. |
向某溶液中加入盐酸 |
产生无色气体 |
溶液中一定含有CO32− |
| B. |
新制Fe(OH)2露置于空气中一段时间 |
白色固体迅速变为灰绿色,最终变为红褐色 |
说明Fe(OH)2易被氧化成Fe(OH)3 |
| C. |
在CuSO4溶液中加入KI溶液,再加入苯,振荡 |
上层呈紫红色,下层有白色沉淀生产 |
铜离子可以氧化碘离子,白色沉淀可能为CuI |
| D. |
向某无色溶液中滴加硝酸酸化的BaCl2溶液 |
产生白色沉淀 |
溶液中一定含有SO42- |