用NA表示阿伏加德罗常数。下列叙述正确的是
| A.1.0L0.1mol/L的NH4Cl溶液中NH4+的个数为0.1NA |
| B.常温下,Cu-Zn原电池中,正极产生1.12LH2时,转移的电子数为0.1NA |
| C.常温下,0.05molCO2和SO2混合气体中所含氧原子数为0.1NA |
| D.高温高压下,1.4 g N2与0.3 g H2反应,生成的NH3分子数为0.1NA |
食品卫生与身体健康密切相关,下列物质可以用作食品添加剂的是
| A.三聚氰胺 | B.苏丹红 | C.甲醇 | D.柠檬酸钠 |
某溶液中可能含有下列离子:Na+、Fe2+、NH4+、Cl-、SO32-、SO42-、NO3-和NO2-等,将该溶液分成4份,进行如下实验:
第一份滴加适量的淀粉KI溶液,呈蓝色;
第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;
第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;
第四份加入足量硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。
下列说法正确的是
| A.该溶液中肯定存在的离子有NH4+、SO42-、NO2- |
| B.该溶液中肯定存在的离子有NH4+、Cl-、NO3- |
| C.该溶液中肯定不存在Fe2+、SO32-、NO2- |
| D.该溶液中可能存在Na+、Fe2+、Cl- |
关于下列各图的叙述,正确的是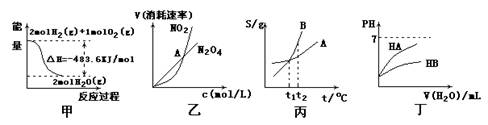
A.甲表示2molH2(g)所具有的能量一定比2mol气态水所具有的能量多483.6KJ B.乙表示恒温恒容条件下发生的可逆反应2NO2N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
B.乙表示恒温恒容条件下发生的可逆反应2NO2N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将t1℃时的A、B饱和溶液分别由
t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同温同浓度的NaA溶液的pH小于NaB溶液的Ph
.在体育比赛中使用兴奋剂是一种不符合奥林匹克精神的行为,某种兴奋剂的结构简式如右图所示,有关该物质的说法中正确的是 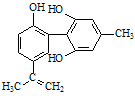
| A.分子内所有原子可能在同一平面上 |
| B.该物质可发生取代、加成、消去、氧化、加聚等有机反应类型 |
| C.1mol该物质与足量H2反应后的产物不能与NaOH溶液反应 |
| D.若能使酸性KMnO4溶液的紫色褪去,则可证明该物质分子中是否含有碳碳双键 |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
下列有关判断中不正确的是
| A.溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B.若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| C.方案一可能产生氢气,方案二可能剩余铜 |
| D.实验室中方案Ⅱ更便于实施 |