试回答下列中学化学实验中常见仪器的有关问题:
(1)在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同) ;标有使用温度的仪器是 。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器①试管、②分液漏斗、③细口试剂瓶、④广口试剂瓶、⑤集气瓶、⑥滴瓶、⑦酸式滴定管、⑧碱式滴定管中,用到“磨砂”的有 。
(3)在仪器①漏斗、②容量瓶、③蒸馏烧瓶、④分液漏斗、⑤烧杯、⑥蒸发皿中,可用于粗盐提纯实验的有 ;可用于分离两种沸点接近且互不相溶的
液态混合物实验的有 。
下列冶炼金属的对应关系中错误的是()
| 金属冶炼 |
冶炼方法 |
|
| A |
火烧孔雀石 |
焦炭法 |
| B |
湿法炼铜 |
水煤气法 |
| C |
铝热法炼铬 |
活泼金属置换法 |
| D |
光卤石炼镁 |
电解法 |
某些化学试剂可用于净水。水处理中使用的一种无机高分子混凝剂的化学式可表示为[Al2(OH)nClm·yH2O]X,式中m等于()
| A.6-n | B.3-n | C.6+n | D.3+n |
从海水中提取的溴占世界产溴量的1/3。已知溴水呈橙色,将SO2气体通入溴水时,可以观察到溴水褪色。则下列有关叙述中正确的是()
| A.SO2使溴水褪色,显示了SO2的漂白性 |
| B.SO2是形成酸雨的唯一原因 |
| C.从溴水中提取单质溴,可以用乙醇进行萃取 |
| D.SO2使溴水褪色,显示了SO2的还原性 |
某溶液经分析只含有Na+、K+、Ca2+、Cl-、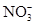 ,已知其中Na+、K+、Ca2+、
,已知其中Na+、K+、Ca2+、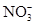 的浓度均为0.2mol·L-1,则Cl-的物质的量浓度为( )
的浓度均为0.2mol·L-1,则Cl-的物质的量浓度为( )
| A.0.6mol·L-1 | B.0.5mol·L-1 | C.0.4mol·L-1 | D.0.3mol·L-1 |
已知Q与R的摩尔质量之比为9∶22,在反应X+2Y====2Q+R中,当1.6 g X与Y完全反应后,生成4.4 g R,则参与反应的Y和生成物Q的质量之比为()
| A.46∶9 | B.32∶9 | C.23∶9 | D.16∶9 |