已知T℃,PkPa时,在容器甲和容器乙中分别充入1mo1A(g)和1 molB(g),发生反应A(g)+B(g) C(g) DH<0,反应过程中温度保持不变。已知起始时V乙
C(g) DH<0,反应过程中温度保持不变。已知起始时V乙
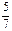 V甲,装置如下图所示。当反应达平衡时,测得甲中C的体积分数为40%。下列说法中不正确的是
V甲,装置如下图所示。当反应达平衡时,测得甲中C的体积分数为40%。下列说法中不正确的是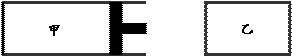
| A.容器甲、乙中反应的起始速率不等 |
| B.达平衡时,容器甲、乙中各组分的体积分数不等 |
| C.达平衡时,容器甲、乙中放出的热量相等 |
| D.达平衡时,容器乙中再充入少量稀有气体,A的转化率不变 |
下列有关金属的工业制法中,正确的是
| A.制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中的铁 |
| C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| D.炼铜:用黄铜矿(主要成分为CuFeS2)直接电解精炼得到纯度为99.9%的铜 |
下列离子方程式的书写正确的是
| A.铁和稀硝酸反应:Fe + 2H+ = H 2↑+ Fe 2+ |
| B.NaHCO3溶液与NaOH溶液反应: OH- + HCO3-= CO32-+ H2O |
| C.氯化铝溶液与足量氨水反应:Al3++ 4OH-=AlO2-+2H2O |
| D.硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓ |
在CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,发现铁钉并无任何变化。根据上述现象,确定下面结论正确的是()
| A.不溶物一定是Cu | B.不溶物一定含铜,但不一定含铁 |
| C.不溶物一定是Fe | D.溶液中一定含有Fe2+,但不一定含有Cu2+ |
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子可能是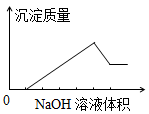
| A.Mg2+、Al3+、Fe3+ | B.Na+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.H+、Mg2+、Al3+ |
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
| A.KClO3是氧化剂 | B.被氧化与被还原的氯元素的质量比为5:1 |
| C.H2SO4既不是氧化剂又不是还原剂 | D.1mol KClO3参加反应时有10mol电子转移 |