肼(N2H4)又称联氨,是一种可燃性液体,用作火箭燃料。
(1)32.0g该液态化合物在氧气中完全燃烧生成氮气放出热量624kJ(25°C,101kPa),则肼完全燃烧的热化学方程式 。
(2)肼——空气燃料电池是一种无污染的清洁的碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,作负极的燃料是 (填化学式);正极的电极反应式是 。
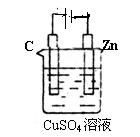
(3)右图是一个电化学过程示意图。
①锌片上发生的电极反应是________________________。
②假设使用肼一空气燃烧电池作为本过程中的电源,锌片的质量
变化是128g,则肼一空气燃料电池理论上消耗标准状况下的空气_____L
(假设空气中氧气体积含量为20%)
8分)下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上。
| 品 名 |
×××××× |
| 配 料 |
精炼植物油、鲜鸡蛋、精面粉、碳酸氢钠、日落黄、甜蜜素、山梨酸钾等 |
| 保质期 |
90天 |
| 生产日期 |
标于包装袋封口上 |
(1) 富含蛋白质的是_________ _______ (2)富含糖类的是______________
_______ (2)富含糖类的是______________
(3)富含油脂的是_________________(4)属于防腐剂的是
在一定体积密闭容器中,进行如下反应: CO2(g
CO2(g ) + H2(g)
) + H2(g)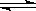 CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1) K的表达式为:
(2) 该反应为 反应(“吸热”或“放热”)
(3) 能判断该反应是否达到化学平衡状态的依据
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4)在830℃时,若起始浓度c(CO)为1mol·L—1,c(H2O)为1mol·L—1,反应达到平衡时,CO的转化率为。
铅蓄电池是化学电源,它工作时的电池反应为:PbO2+Pb+2H2SO4===2PbSO4+2H2O。试回答:
(1)铅蓄电池正极的电极材料是__________。
(2)工作时该铅蓄电池负极的电极反应是__ ___________________________________。
(3)铅蓄电池工作时,电解质溶液的密度__________(填“减小”“增大”或“不变”,下同),pH__________。
(4)如果用铅蓄电池做电源电解饱和食盐水制取Cl2,当制得0.05 mol Cl2时,在理论上电池内部消耗的H2SO4的物质的量是____________。
(1)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是。
(2)利用右装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应该置于处。若X为锌,开关K置于M 处,该电化学防护法称为。
处,该电化学防护法称为。
如图所示,若电解5 min 时铜电极质量增加2.16 g,试讨论:
时铜电极质量增加2.16 g,试讨论: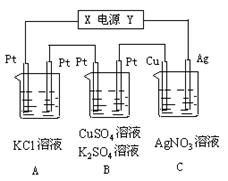
⑴电源电极X名称为_________。
⑵ pH变化:A_______,B______,C______。
⑶通过5 min时,B中共收集224 mL气体(标况),溶液体积为200mL,则通电前硫酸铜溶液的物质的量浓度为______________。
⑷若A中KCl溶液的体积也是2 00 mL,且电解过程中体积不变,电解后溶液中的氢氧根离子浓度是__________
00 mL,且电解过程中体积不变,电解后溶液中的氢氧根离子浓度是__________ 。
。