MnSO4·H2O在工业、农业等方面有广泛的应用。
(一)制备:工业上用化工厂尾气中低浓度SO2还原MnO2矿制备MnSO4·H2O过程如下:
已知:常温时部分硫化物难溶盐的Ksp:CuS--6.3×10-36、PbS--1.0×10-28、NiS--2.0×10-26、MnS--2.5×10-10,请回答下列问题:
(1)生产中MnO2矿粉碎的目的是 。(2)除铁发生的离子反应方程式为 。
(3)除重金属离子后,若混合溶液中Cu2+、Pb2+、Ni2+的浓度均为1.0×10-5mol/L,则c(S2-)最大= mol/L。
(二):性质—热稳定性:MnSO4·H2O在1150℃高温下分解的产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是
(三)废水处理:工厂废水中主要污染为Mn2+和Cr6+,现研究铁屑用量和pH值对废水中铬、锰去除率的影响,(1)取100mL废水于250 mL三角瓶中,调节pH值到规定值,分别加入不同量的废铁屑.得到铁屑用量对铬和锰去除率的影响如下图1所示。则在pH一定时,废水中铁屑用量为 时锰、铬去除率最好
(2)取100mL废水于250 mL三角瓶中,加入规定量的铁粉,调成不同的pH值。得到pH值对铬和锰去除率的影响如下图2所示。则在铁屑用量一定时,废水pH= 时锰、铬去除率最好
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和H2O2混合反应,生成氮气和水蒸气,放出akJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为。
(2)又已知H2O(l)=H2O(g) ΔH=+bkJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是kJ。(用含a、b的代数式表示,请化简)
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
有机物A是一种广谱高效食品防腐剂,下图是A 分子的球棍模型。回答问题: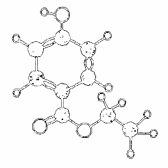
(1)写出A的分子式:;
(2)A不能够发生反应的类型有(填写序号):;
① 水解反应② 加成反应
③ 取代反应④ 消去反应
(3)写出A与烧碱溶液反应的化学方程式:;
(4)下列是一些中草药中所含的有机物:
①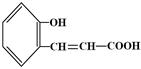 ②
②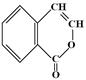 ③
③ ④
④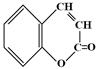
桂皮酸异香豆素二氢异香豆素香豆素
其中互为同分异构体的是(填写序号):;
不能与Br2水反应的是(填写序号):;
(5)A的一种同分异构体B在一定条件下可转化为二氢异香豆素,B的结构简式为_________,B能否发生消去反应(填“能”或“不能”);
(6)A的另一种同分异构体C遇FeCl3溶液显紫色;1molC可与1mol NaOH反应生成有机物D;D被Ag(NH3)2OH溶液氧化后经酸化得有机物E,E经酯化、消去两步反应可得香豆素。写出符合上述要求的一种C的结构简式:
______________________________________________________________
21分)有以下一系列反应,最终产物为草酸(乙二酸)。
B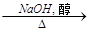 C
C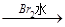 D
D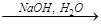 E
E F
F
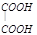 ,已知B为某一溴代物。
,已知B为某一溴代物。
(1)推测用字母代表的化合物的结构式:C____________,F ______________。
(2)写出化学方程式:B→C____________________。E→F_______________。
(3)E和草酸在一定条件下生成的环状化合物的结构简式为。
(4)写出E和草酸在一定条件下生成高分子化合物的化学方程式。
14分)硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3MgO、CaO等,生产工艺流程示意如下:
(1)将菱锌矿研磨成粉的目的是。
(2)完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3 +□Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学相对分子质量为89,化学式是_______。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______。
| Mg(OH)2 |
Zn(OH)2 |
MgCO3 |
CaCO3 |
|
| 开始沉淀的pH |
10.4 |
6.4 |
— |
— |
| 沉淀完全的pH |
12.4 |
8.0 |
— |
— |
| 开始溶解的pH |
— |
10.5 |
— |
— |
| Ksp |
5.6×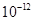 |
— |
6.8×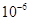 |
2.8×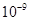 |
(5)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(6)抽滤装置如下图所示,该装置中的错误之处是___________;抽滤完毕或中途需停止抽滤时,应先_________________________,然后_______________________。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________。
食醋分为酿造醋和配制醋两种。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)某研究小组利用滴定分析法测定某品牌食醋中醋酸的含量,下列说法正确的是。
a.用NaOH溶液滴定时反应的离子方程式为:H++OH-=H2O
b.食醋试样需稀释一定倍数后再进行滴定
c.用NaOH溶液滴定食醋,可使用酚酞或甲基橙作指示剂
d.若测得该品牌食醋的物质的量浓度为0.75mol·L-1,则该食醋的总酸量为4.5g/100mL。
(2)研究小组的同学仔细观察了该品牌食醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与食品添加剂(苯甲酸钠C6H5COONa)不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的(填选项字母)。
a.pHb.电离度c.电离常数d.溶解度
(3)常温下,用0.1000 mol·L-1NaOH溶液分别滴定20.00mL 0.1000 mol·L-1HCl溶液和20.00mL 0.1000 mol·L-1CH3COOH溶液,得到2条滴定曲线,如下图所示。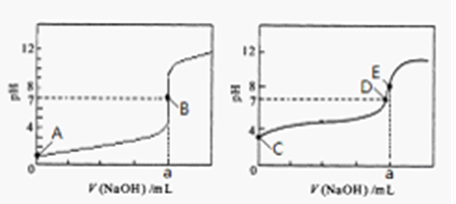
图3图4
①滴定醋酸溶液的曲线是(填“图l”或“图2”);滴定曲线中a=mL
(4)现欲粗略测定一未知浓度的CH3COOH溶液的电离度,应做的实验和所需的试剂(试纸)是。
a.电解,NaOH溶液b.蒸馏,Na2CO3溶液
c.酯化反应,石蕊试液 d.中和滴定,pH试纸图2
(5)酸式滴定管用蒸馏水润洗后,未用标准液润洗,导致滴定结果(填“偏小”、“偏大”或“无影响”);酸式滴定管读数时,若先俯后仰,则结果会。