有机物DBP常用作纤维素树脂和聚氯乙烯的增塑剂,特别适用于硝酸纤维素涂料。具有优良的溶解性、分散性和粘着性。由有机物A和邻二甲苯为原料可以合成DBP。

已知:①RCH=CH2+CO+H2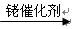

②烃A是有机合成的重要原料。A的质谱图表明其相对分子质量为42,红外光谱表明分子中含有碳碳双键;B能发生银镜反应;有机物c的核磁共振氢谱显示其分子中含有5种氢原子,且其峰面积之比为3:2:2:2:1;DBP分子中苯环上的一溴取代物只有两种。
(1)A的结构简式是  。
。
(2)B含有的官能团名称是 。
(3)有机物C和D反应生成DBP的化学方程式是 。
(4)下列说法正确的是(选填序号字母) 。
a.A能发生聚合反应、加成反应和氧化反应
b.和C互为同分异构体,且含有相同官能团的有机物有2种
c.邻二甲苯能氧化生成D说明有机物分子中基团之间存在相互影响
d.1 mol DBP可与含2 mol NaOH的溶液完全反应
(5)工业上常用有机物E(C8H4O3)代替D生产DBP。反应分为两步进行:
①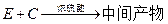 ②
②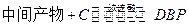
工业生产中在第②步中使用油水分离器将反应过程中生成的水不断从反应体系中分离除去,其目的是 。
(6)工业上生产有机物E的反应如下:
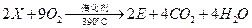
芳香烃X的一溴取代物只有两种,X的的结构简式是 。
环己烷()在负载纳米Au的分子筛(Au/TS1)催化剂的作用下与空气发生氧化反应,反应原理是:通过游离基反 应形成环己基过氧化氢,该过氧化物在Au/TS1催化作用下受热分解,生成环己醇和环己酮(O)。由于环己醇、环己酮比环己烷更容易被氧化,因而有许多副产物(如己二酸及一些酯类化合物)生成。
应形成环己基过氧化氢,该过氧化物在Au/TS1催化作用下受热分解,生成环己醇和环己酮(O)。由于环己醇、环己酮比环己烷更容易被氧化,因而有许多副产物(如己二酸及一些酯类化合物)生成。
(1) 下表是某反应温度下,环己烷催化氧化反应的转化率(x)和目标产物的选择性(S)的结果:
| 催化剂 |
转化率(x)/% |
|||
| 目标产物的选择性(S)/% |
||||
| 环己基过氧化氢 |
环己醇 |
环己酮 |
||
| Au/TS1 |
10.4 |
14.1 |
34.9 |
39.8 |
① 写出环己烷催化氧化为环己酮的化学方程式: 。
② 若在反应容器中加入1.0mol环己烷,则生成的环己酮的物质的量为________(保留2位小数)。
(2) 图甲是反应温度对环己烷催化氧化反应的转化率(x)和目标产物的选择性(S)和目标产物的总收率(y)的影响。
① 由图甲可知:该反应较适宜的反应温度为________左右。
② 随着反应温度的升高,环己烷的转化率(x)逐渐增加,而目标产物的选择性(S)和 目标产物的总收率(y)却逐渐降低,其可能的原因是 。
目标产物的总收率(y)却逐渐降低,其可能的原因是 。
(3) 图乙是反应时间对环己烷催化氧化反应的转化率(x)和目标产物的选择性(S)和目标产物的总收率(y)的影响。
① 由图乙可知,该反应较适宜的反应时间为________左右。
② 随着反应时间的延长,环己烷的转化率(x)逐渐增加,而目标产物的选择性(S)逐渐降低,这说明________________________________________________________。
在探索生命奥妙的过程中,科学家们日益认识到生命细胞的组成和元素周期律有密切的关系。已知:①人体中不含稀有气体元素;②约占人体总质量99.97%的11种宏量元素,除K、Ca外,其余都为短周期元素;③其余0.03%是由十多种人体不可缺少的微量元素组成。在微量元素中,只有F和Si位于短周期,其余均在第一长周期。请根据试题要求,在11种宏量元素的8种元素中(除H、N、P外),选择合适元素填空:
(1)有一种元素A,其原子最外层电子数是内层电子数的2倍。则A处于元素周期表的位置为。
(2)有一种元素B,它的最高价氧化物对应的水化物是已知酸中酸性最强的酸,该酸的化学式为。宏量元素C是一种非金属元素,它与B处于同一周期,则C的原子结构示意图为。
(3)所有宏量元素中,元素D金属性最强 ,则D为(填元素符号)。除钙元素外,元素E也与D相邻。则E的单质与水反应的离子方程式为。
,则D为(填元素符号)。除钙元素外,元素E也与D相邻。则E的单质与水反应的离子方程式为。
(4)除A—E和钙元素外,还有两种宏量元素F、G。已知它们的离子的电子层结构相同,且带电量也相同但符号相反。F、G的离子中,半径较大的是(填离子符号)。
一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质,不溶于水,也不溶于一般有机溶剂。能发生如下变化(A-F均分别代表一种物质,框图中的部分产物已略去)
|


图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其中A为单质;在实验室中,常用固体B和固体C加热制取气体F;F与G的组成元素相同,G与I分子所含电子数相同。请回答: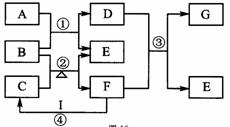
(1)写出B、G的化学式B、G。
(2)写出C的电子式;反应④的实验现象为;写出F的一种具体用
途。
(3)向具有漂白作用的D溶液加入I的稀溶液,写出反应的离子方程式:
。
向D的溶液加入I的浓溶液有A生成,其反应的离子方程式为:
。
(4)写出反应③的化学方程式。
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水。向该盐的溶液中滴加足量的盐酸,随着盐酸的逐滴加入,所观察到的现象是,反应结束时,该反应的总反应离子方程式为。
(2)W与Y可形成化合物W2Y,该化合物的水溶液显_性,原因(用离子方程式表示)__________________________;它的水溶液中存在多种离子,请写出电荷守恒的等式。
(3)若甲为W的最高价氧化物对应的水化物,乙为Y的氢化物。
现有①0.2mol/甲的溶液和②0.2mol/L乙的溶液,则①中由水电离出c(OH-)
_____②中由水电离出的c(OH-)。(填“>”、“=”或“<”)
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
。