将石墨置于熔融的钾中,石墨会吸收钾而形成称为钾石墨的物质,其组成是C8K、C24K、C36K、C48K和C60K。在钾石墨中,钾元素处于石墨中间层,因而石墨层之间被胀大,层间距离增大,钾原子把最外层电子交给石墨层但在遇到与金属钾易反应的其它物质时还会收回。下列对钾石墨的叙述正确的是
| A.钾石墨是一类共价化合物 | B.钾石墨导电性比石墨强 |
| C.钾石墨遇水不产生氢气 | D.C8K、C24K和C36K属于同素异形体 |
下列实验装置或操作与粒子的大小无直接关系的是 ( )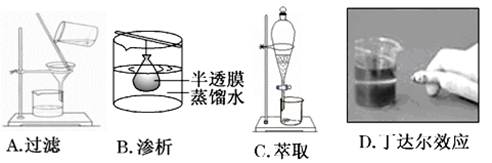
目前有研究表明,过氧乙酸对甲型H1N1流感病毒有较好的杀菌作用,这主要是利用了过氧乙酸的()
| A.酸性 | B.强氧化性 | C.还原性 | D.挥发性 |
关于图中四个图像的说法正确的是(注:图中,E表示能量,p表示压强,t表示时间,V表示体积,B%表示B的体积百分含量。)()
A.①表示化学反应H2(g)+Cl2(g) =2HCl(g)的能量变化,则该反应的反应热△H ="183" j/mol |
B.②表示其它条件不变时,反应4A(g)+3B(g) 2C(g)+6D在不同压强下B%随时间的变化,则D-定是气体 |
| C.③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D.④表示10 mL O.lmol/L NaCO3和NaHCO3两种溶液中,分别滴加0.lmol/L HCl产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
下列判断中一定正确的是()
| A.若X、Y属于同主族元素,且相对原子质量:X>Y,则X失电子能力比Y的强 |
| B.若R2-和M+的电子层结构相同,则原子序数:R>M |
| C.若X、Y都是气态氢化物,且相对分子质量:X>Y,则沸点:X>Y |
| D.若M,N是同主族元素,且原子序数:M>N,则非金属性:M>N |
在1 100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g)△H="a" kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是()
| A.若生成1 mol Fe,则吸收的热量小于akJ |
| B.若要提高CO的转化率,则应该加入适当的过量Fe0 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |