某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
|
||||
 |
||||

| 实验序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
溶液褪色 |
氯气与水反应的产物有漂白性 |
| Ⅱ |
氯水中加入 NaHCO3粉末 |
有无色气泡产生 |
氯气与水反应的产物具有较强的酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由。
。
② 请利用上述装置设计一个简单的实验,验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2
并进行有关实验。
① B中发生反应的化学方程式为 。
② 欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是 。
③ 试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是 (气体按标准状况计算)。
(10分)已知某溶液中存在OH-、H+、NH4+、Cl- 四种离子。某同学推测其离子浓度大小顺序有如下关系:
①.c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③.c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是_____________________(填化学式)上述四种离子浓度的大小关系为_____________(填序号)
(2)若上述关系中③是正确的,则溶液中的溶质为_____________________(填化学式)
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)______________c(OH-)
(6分)下列实验操作,最终得到的固体物质为 (填化学式)
(1)将K2CO3溶液蒸干____________________________
(2)将Na2SO3溶液蒸干___________________________
(3)将AlCl3溶液蒸干并灼烧_______________________
(10分)今有①CH3COOH ②HCl ③H2SO4三种溶液。根据要求回答下列问题:
(1)当它们pH相同时,其物质的量浓度由大到小排列是________________(填序号)
(2)当它们的物质的量浓度相同时,其pH由大到小的顺序是______________(填序号)
(3)中和等量的同一烧碱溶液,需相同的物质的量浓度的①②③三种酸溶液的体积比为
___________________________________。
(4)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱的体积比为_____________________;此时所得到的三种溶液的pH大小关系为______________________。
[化学 选修5-有机化学基础] (共14分)有机化合物A、B、C、D完全燃烧均只生成CO2和H2O,且四种物质含碳质量分数均为40%,含氢质量分数均约6.7% 。又知:
①A常温、常压下呈气态,A、C都能发生银镜反应,但都不能发生水解反应;
②B和C互为同分异构体,l mol B完全燃烧需耗3mol氧气。核磁共振氢谱表明,B分子有四个吸收峰,且峰面积之比为3:1:1:1,B在浓硫酸存在下加热可生成W(C6H8O4,含有一个六元环);
③ RCOOH在一定条件下可被还原为RCHO,以下是由B制取C的一种合成路线(反应条件及副产物已略去):
试回答:
(1)A含有的官能团名称为
(2)B的结构简式为。反应B→X的化学方程式为。
(3)C与新制的Cu(OH)2反应的化学方程式。
(4)与B互为同分异构体,属于有机酸的酯类且含有羟基的化合物有多种,写出其中一种的结构简式:。
(5)写出Z→C的化学反应方程式:。
(6)若MD =" 6" MA,D是只含有一种官能团且碳原子的化学环境相同的六元环状物,又名肌醇。医学上将肌醇用于动脉硬化、高血脂症、脂肪肝的防治。则D的结构简式为 。
(每空2分,共14分)一化学兴趣小组的同学们对SO2与漂粉精的反应进行实验探究:
| 操作 |
现象 |
| 取4g漂粉精固体,加入100mL水 |
部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH |
pH试纸先变蓝(约为12),后褪色 |
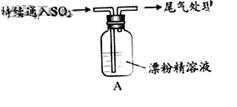 |
1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)C12和Ca(OH)2制取漂粉精的反应中氧化剂与还原剂的物质的量之比为。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是。
(3)向水中持续通入SO2,未观察到白雾。推测现象1的白雾由HC1小液滴形成。
①HC1的电子式是。
②兴趣小组将A中产生的白雾引出导入硝酸酸化的硝酸银溶液中,结果有沉淀产生,有同学据此判断白雾确为HC1小液滴,试评价该结论的合理性并说明理由。
(4)现象2中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和C1-发生反应。通过进一步实验确认了这种可能性,其实验方案是。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaC12溶液,产生白色沉淀。则沉淀X中含有的物质是。
②用离子方程式解释现象3中黄绿色褪去的原因:。