绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:

已知:室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)检验制得的绿矾晶体中是否含有Fe3+的实验操作是
________________________________________________________。
(2)操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至pH=2的目的是 。
(3)操作IV的顺序依次为: 、冷却结晶、 。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL(滴定时发生反应的离子方程式为:5Fe2++MnO4¯+8H+→5Fe3++Mn2++4H2O)。
①判断此滴定实验达到终点的方法是 。
②计算上述样品中FeSO4·7H2O的质量分数为 (用小数表示,保留三位小数)。
③若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有 ; 。
实验题:现有药品:W g(W<1)锌片、稀硫酸、无水硫酸铜、氧化铜和水。请从图中选用适当的实验装置,设计一个简单的实验,粗略测定锌的相对原子质量(假设环境为标准状况)。
(1)应选用的装置是(只要求写出图中装置的标号)。
(2)所用装置的连接顺序是(填各接口的字母,胶管省略)。
(3)为了保证不漏出氢气,操作中加放试剂 的方法是。
的方法是。
(4)用实验所测得的数据,写出计算锌的相对原子质量的数学式:Mr(Zn)=。
(8分)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:
 ①2Mg+O2
①2Mg+O2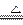 2MgO;
2MgO;
②3Mg+N2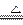 Mg3N2;
Mg3N2;
③2Mg+CO2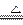 2MgO+C;
2MgO+C; ④Mg+H2O
④Mg+H2O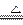 MgO+H2↑;
MgO+H2↑;
⑤Mg3N2 +6H2O =3Mg(OH)2↓+2NH3↑
 可供选择的装置和药品如上图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
可供选择的装置和药品如上图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。 回答下列问题
回答下列问题



 (1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)。
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)。 (2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)。
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)。 (3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?
,原因是。 (4)请设计一个实验,验证产物是氮化镁:。
(4)请设计一个实验,验证产物是氮化镁:。
(8分)某研究性学习小组为证明在同温同压下,相同浓度、相同体积酸性不同的两种二元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图所示.该实验的主要操作步骤如下:
Ⅰ.①配制浓度均为0.5 mol/L 的H2SO4和H2C2O4溶液。
②用 量取10.00 mL 0.5 mol/L H2SO4和H2C2O4溶液分别于两个锥形瓶中.
③分别称取除去表面氧化膜的镁带并系于铜丝末端。
④检查装置的气密性,在广口瓶中装满水,按图连接好装置。
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触)至反应完全后,记录 。
⑥反应结束后,读取量筒内水的体积为y mL。
Ⅱ.请将上述步骤补充完整并回答下列问题:
(1)用密度为1.84 g/cm3 98%的浓H2SO4,配制浓度为250 mL 0.5 mol/L的H2SO4溶液,所需要的主要仪器有 、 、烧杯、玻璃棒、酸式滴定管。
(2)以下是读取量筒内水的体积时,必须包括的几个步骤:①使乙、丙中液面相平;②将装置冷却至室温;③读取量筒内水的体积.这三步操作的正确顺序是 。
(3)读取量筒内水的体积时,若丙中液面高于乙中液面,使乙、丙中液面相平的操作是 。
(4)简述速率不等的原因 ,
铜丝不与酸接触的原因 。
如图所示,A是制取溴苯的实验装置,B、C是改进后的装置。请仔细分析,对比三个装置,回答下列问题: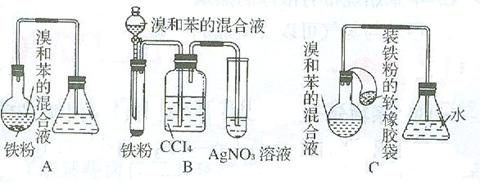
(1)写出三个装置中共同发生反应的化学方程式:___________________
(2)装置A和C均采用了长玻璃导管,其作用是_____________________________
(3)按装置B、C装好仪器及药品后,要使反应开始,应对装置B进行的操作是_________,应对装置C进行的操作是 ___________________________________。
(4)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作,装置A中这一问题在实验中造成的后果是________________________。
(5)B中采用了洗气瓶吸收装置,反应后洗气瓶中可能出现的现象是_______
(10分)实验室用乙醇与浓硫酸共热制取乙烯,常因温度过高生成少量SO2,有人设计了如下图所示实验,以验证上述混合气体中是否含有乙烯和SO2。
(1)装置中X仪器的名称是:;
碎瓷片的作用是:。
(2)写出生成乙烯的化学反应方程式:。
(3)A、B、C、D装置中可盛放的试剂是(从下列所给试剂中选出,填序号):
①品 红溶液,②NaOH溶液,③溴水,④KMnO4酸性溶液。
红溶液,②NaOH溶液,③溴水,④KMnO4酸性溶液。
A.;B.;C.;D.。
(4)能说明SO2气体存在的现象是。
(5)确证含有乙烯的现象是。