S O2与O2在催化剂作用下合成SO3的反应为:2SO2(g)+O2(g)  2SO3(g)。在容积均为1L的a、b、c、d、e五个密闭容器中均充入1mol O2和2mol SO2混合气体,控温。反应进行5min时,测得相关数据如下表:
2SO3(g)。在容积均为1L的a、b、c、d、e五个密闭容器中均充入1mol O2和2mol SO2混合气体,控温。反应进行5min时,测得相关数据如下表:
 容器温度 容器温度浓度 |
a容器 400℃ |
b容器 425℃ |
c容器 450℃ |
d容器 475℃ |
e容器 500℃ |
| c(O2) |
0.8 |
0.6 |
0.3 |
0.5 |
0.7 |
| c(SO3) |
0.4 |
0.8 |
1.4 |
1.0 |
0.6 |
(1)反应进行5min内,五个容器中平均反应速率最大的是_______________(填容器编号);
(2)计算a容器中O2的反应速率_________________;
(3)写出该反应的平衡常数表达式K=___________________,比较上表中数据,推测可能达到平衡的容器是_____________(填容器编号);
(4)该反应是________(填“放热”、“吸热”)反应,在右图坐标中画出e容器中SO3的物质的量随时间的变化
曲线。
防止水体污染,改善水质,最根本的措施是控制工业废水和生活污水的排放。有一种工业废水,已知其中含有大量的Fe2+和SO42-,少量的Ag+ 以及部分污泥。某校化学兴趣小组同学通过下列操作过程,回收物质,处理废水。
根据上述操作过程,回答下列问题:
|
(1)在实验室进行①操作时,需要的主要玻璃仪器有 。
(2)操作②的名称是 。根据正放在桌面上的右图装置,回答下列问题: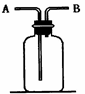
(1)现有H2、SO2、NH3、N2四种气体
①用排空气法收集某气体,则由A口进气可收集到的气体为。
②用排水法收集某气体,可在该容器中充满水,气体应由口进入。
(2)若用该装置除去H2中的水分,容器中可盛放的试剂为。
A、B、C、D四种元素均为短周期元素,其原子半径依次减小,它们的气态氢化物分子所含的电子数相同,C元素原子的最外层电子数是内层电子数的3倍。根据以上信息,按要求填空。
(1)A的最高价氧化物的电子式。
(2)D在周期表中的位置。
(3)在25℃、101KPa下,已知1g A的气态氢化物在足量氧气中燃烧后恢复到原状态,放出55.6KJ的热量,该反应的热化学方程式。
(1)写出碳酸钙与醋酸反应的离子方程式:。
(2)乙烯通入溴水中的化学方程式:。
目前市场销售的某种食用精制盐包装袋上有如下说明:
| 产品标准 |
GB5461 |
| 产品等级 |
一级 |
| 配料 |
食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) |
20~50mg/kg |
| 分装日期 |
|
| 分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)KIO3+KI+H2SO4=K2SO4+I2+H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是。
②某学生设计回收四氯化碳的操作步骤为:
a将碘的四氯化碳溶液置于分液漏斗中;
b加入适量Na2SO3稀溶液;
c分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a准确称取wg食盐,加适量蒸馏水使其完全溶解;
b用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c以淀粉为指示剂,逐滴加入物质的量浓度为1.00×10-3mol·L-1的Na2S2O3溶液24.00mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是。
②b中反应所产生的I2的物质的量是mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)mg/kg。