国家游泳池水质标准:
| 游离性余氯 |
0.3~0.5 mg·L-1 |
| pH |
6.5~8.5 |
| 浑浊度 |
≤5度 |
| 细菌总数 |
≤1 000个/mL |
| 大肠菌群 |
≤18个/mL |
| 硫酸铜剂量 |
0.25~0.50 mg·L-1,最大加药量不超过1.0 mg·L-1 |
*游离性余氯:包括ClO-及HClO等。
请参考表中有关信息回答以下问题:
(1)游泳池一般用漂白精作为消毒剂,漂白精的有效成分是Ca(ClO)2,其消毒原理是_________________________________。
(2)池中加入硫酸铜的目的是__________________,如果加入硫酸铜的剂量过大会对人体产生有害作用,其原因是什么?_________________________________。
(3)某游泳池注满水,水的总体积为1.50×103 m3,该游泳池消毒一次所用的漂白精,理论上需用多少升标准状况下的氯气和多少克氢氧化钙来制取?(列式计算)(池水的密度为1.00 g·cm-3,游离性余氯按ClO- 0.50 mg·L-1计)
生活和生产中常用到胶体的性质,请看下述四例:
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁溶液应急止血,其原理是
_______________________________________________。
(2)在陶瓷工业上常遇到因陶土里混有氧化铁而影响产品质量。解决方法之一是把这些陶土和水一起搅拌,使微粒直径在10-9~10-7m之间,然后插入两根电极,再接通直流电源。这时阳极聚集陶土胶粒,阴极聚集氧化铁胶粒,理由是________。
(3)水泥和冶金工厂常用高压电对气溶胶作用以除去大量烟尘,减少对空气的污染,这种作用运用了________原理。
(4)四氧化三铁在强碱性溶液中与次氯酸盐反应,生成高铁酸盐(FeO42—),FeO42—有强氧化性,可以杀菌消毒。高铁酸盐还有净化水的作用,能净化水的原因是 ______________________________________________________
已知A、B,C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下图进行反应。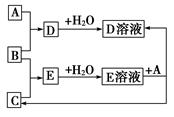
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的________,理由是________。
(3)如果E溶液是一种强酸,则E的化学式为________。
无机化合物可根据其组成和性质进行分类:
(1)下图所示的物质分类方法名称是________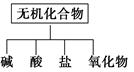
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
| 化学式 |
HCl②____ |
③___④Ba(OH)2 |
⑤Na2CO3⑥____ |
⑦CO2⑧Na2O2 |
(3)写出⑦转化为⑤的化学方程式_____________________________
(4)呼吸面具中用⑧作为O2来源的反应原理为:___________________________
(5)实验室制备⑦常用________和________反应,检验该气体的方法是____________
对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。
(1)现有下列6种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2。按照不同的分类标准,它们中有一种物质与其他5种有明显的不同,请找出这种物质,并写出依据(写出两种分类方法):
①________________________________。
②________________________________。
(2)从上述物质中分别找出两种能相互反应的物质,各写一个非氧化还原反应的方程式和氧化还原反应的方程式__________________________________________________
(3)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,请用简单的图示方法表示二者之间的关系:___________________________。
(4)生活中的食醋和淀粉溶液分别属于分散系中的________和________,用________可以鉴别(填化学专用名词)。
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题: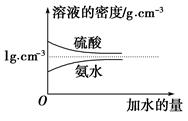
| 溶质的物质的量浓度/mol·L-1 |
溶液的密度/g·cm-3 |
|
| 硫酸 |
c1 |
ρ1 |
| 氨水 |
c2 |
ρ2 |
(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为________mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与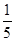 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________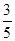 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。