有机物A的分子结构为,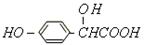 写出A实现下列转变所需的药品
写出A实现下列转变所需的药品
(1)A转变为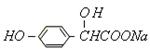 ,
,
(2)A转变为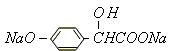 ,
,  (3)A转变为
(3)A转变为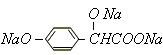 ,
,
漂白粉是一种很好的消毒剂和漂白剂。制取漂白粉是用___________和____________反应,请写出其化学方程式__________________________________________。漂白粉的有效成分是__________。漂白粉在空气中很容易变质,请写出漂白粉在空气中变质的机理(写反应方程式)_____________________________________________________ 。
常温下,A是双原子分子气态单质,显黄绿色,M为71g/mol,B、C、D都是含A元素的化合物,转化关系如图所示[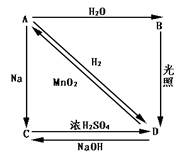
⑴分别写出A、B、C、D的化学式 :
: A; B;
A; B;
C; D。
⑵写出A→B、C→D的化学方程式:
A→B;
C→D。
A元素原子M电子层上有6个电子。B元素与A元素的原子核外电子层数相同,B元素的原子最外电子层只有1个电子。
⑴ B元素的原子结构示意图为___________________;A元素原子的电子式___________;
⑵ A、B两元素形成的化合物的名称是____________,化学式是___________________。
等质量的SO2和SO3分子数之比为,氧元素质量之比为。同质量的氨气和硫化氢气体中所含氢原子个数比是,若两者所含氢原子个数相等,它们的物质的量比是。
在原子结构的探索过程中,很多科学家作出了相应的贡献,我国古代的认为物质是无限可分的,近代原子学说是由提出的,发现了铀的放射性,卢瑟福通过实验,提出了原子结构的行星模型。