如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池,关于该原电池的叙述正确的是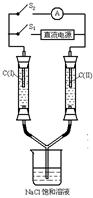
| A.C(Ⅰ)的电极名称是阴极 |
| B.C(Ⅱ)的电极名称是负极 |
C.C(Ⅰ)的电极反 应式是2H++2e-=H2↑ 应式是2H++2e-=H2↑ |
| D.C(Ⅱ)的电极反应式是Cl2+2e-=2Cl- |
常温下,下列有关醋酸溶液的叙述中不正确的是()
| A.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO—) |
| B.浓度均为0.1mol/L的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO—)- c(CH3COOH)=2[c(H+)- c(OH—)] |
C.将pH=a的醋酸稀释为pH=a+1的过程中, 不变 不变 |
| D.0.2mol/L的CH3COOH溶液中c(H+)与0.1mol/LCH3COOH溶液中c(H+)的比值小于2 |
16mL由NO与NH3组成的混合气体在催化剂作用下于400℃左右可发生反应6NO+4NH3====5N2+6H2O,达到平衡时在相同条件下体积变为17mL,则原混合气体中NO与NH3的体积比可能是()
①3:1 ②3:2 ③3:4 ④3:5
| A.①② | B.①④ | C.②③ | D.③④ |
下列事实不能用平衡移动原理来解释的是()
| A.打开啤酒瓶盖,产生大量气泡 |
| B.稀释CH3COOH时,溶液中CH3COO—数目增多 |
| C.工业合成氨常用500℃左右的温度 |
| D.热的纯碱溶液的去污效果比冷的好 |
设NA表示阿伏加德罗常数的数值,下列叙述不正确的是()
| A.常温常压下,1molCO2和CO混合气体中含有的碳原子数为NA |
| B.在KIO3+6HI====KI+3I2+3H2O反应中,每生成3molI2,则转移6NA个电子 |
| C.78gNa2O2与足量CO2完全反应,转移的电子总数为NA |
| D.在1L0.1mol/LNa2S溶液中,阴离子总数大于0.1NA |
下列实验方案能达到目的的()